Рибофлавин
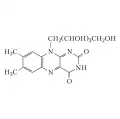
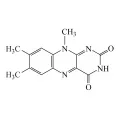
Рибофлави́н [7,8-диметил-10-(1’-D-рибитил)-изоаллоксазин, лактофлавин, овофлавин, витамин B2, Е101], ароматическое соединение, гетероциклическое соединение, производное изоаллоксазина, C17H20N4O6. Рибофлавин был открыт в 1932 г. О. Г. Варбургом и В. Кристианом как составная часть т. н. жёлтого окислительного фермента. Впервые рибофлавин выделили в 1933 г. Р. Кун, П. Дьёрдь и Т. Вагнер-Яурегг из молока (лактофлавин). В 1935 г. П. Каррер осуществил химический синтез рибофлавина из 1-амино-2-карбэтокси-4,5-диметилбензола и D-рибозы. Молярная масса 376,37 г/моль; tпл 282 °C (с разложением).
Физико-химические свойства
Рибофлавин – кристаллическое вещество жёлто-оранжевого цвета, обладающее горьким вкусом, хорошо растворимое в разбавленных щелочах (с разложением), соляной кислоте [1 % в 15%-ной, 4,3 % в 21%-ной, 18 % в 30%-ной (всё при 15 °C)], растворимое в ледяной уксусной кислоте, малорастворимое в воде [0,012 г / 100 мл (27,5 °C), 0,019 г / 100 мл (40 °C), 0,23 г / 100 мл (100 °C)], этаноле [0,045 г / 100 мл (27 °C)], пиридине, феноле, амилацетате, нерастворимое в диэтиловом эфире, ацетоне, хлороформе, бензоле, петролейном эфире.
Показатели констант кислотности (pKa) составляют 3,6 и 9,5.
Насыщенный водный раствор рибофлавина окрашен в жёлто-зелёный цвет с характерной жёлто-зелёной флуоресценцией в видимом и ультрафиолетовом свете.
Сухой кристаллический рибофлавин устойчив к рассеянному свету, однако чрезвычайно фотолабилен в растворах, особенно в щелочных. На свету в разбавленных щелочных растворах образуется люмифлавин, в кислых и нейтральных – люмихром.
В щелочных растворах при нагревании расщепляется пиримидиновый цикл рибофлавина. Рибофлавин устойчив к действию азотной кислоты, брома, перекиси водорода; окисляется хромовой кислотой и перманганатом калия. Дитионитом натрия, амальгамой натрия, цинком в соляной кислоте или при каталитическом гидрировании рибофлавин восстанавливается до бесцветного не обладающего флуоресценцией лейкорибофлавина, который легко окисляется кислородом воздуха до рибофлавина.
С тяжёлыми металлами рибофлавин образует металлохелаты.
Способы получения
В промышленности рибофлавин получают путём химического синтеза из 3,4-ксилидина и рибозы или микробиологически, например с использованием актиномицетов (Ashbya gossypii), дрожжей (Candida famata) или генетически модифицированных бактерий (Bacillus subtilis).
Мировое производство рибофлавина в 2023 г. оценивается в 12,7165 тыс. т (Riboflavin Market – Growth, Trends, and Forecasts (2023–2028 // Researchandmarkets).
Биологические свойства рибофлавина
Биосинтез рибофлавина
Рибофлавин вырабатывается у организмов-автотрофов (многих бактерий, растений) и грибов (плесневые грибы, дрожжи) из гуанозинтрифосфата и рибулозо-5-фосфата при помощи ферментов рибофлавинсинтаз, которые характеризуются высокой степенью сходства внутримолекулярных последовательностей. Биосинтез рибофлавина у растений протекает так же, как у бактерий; у грибов рибофлавиновый путь отличается по ряду реакций.
Животные не умеют синтезировать рибофлавин, который является для них незаменимым витамином, и должны получать его либо из пищи, либо при помощи бактерий, обитающих у них в желудочно-кишечном тракте (например, жвачным животным достаточно рибофлавина, который синтезируется их кишечной микрофлорой, у них нет необходимости получать его дополнительно с пищей).
Рибофлавин как предшественник флавиновых коферментов
У животных поступающий с пищей рибофлавин в цитозоле клеток при помощи фермента рибофлавинкиназы (рибофлавин-5-фосфотрансфераза) фосфорилируется до жизненно важного кофермента флавинмононуклеотида (ФМН) – этот этап имеется у всех живых организмов, независимо от происхождения рибофлавина и объёмов уже имеющегося витамина В2. Далее ФМН метаболизируется до флавинадениндинуклеотида (ФАД) при помощи фермента ФАД-синтазы (ФАД-ацетилтрансферазы). Оба фермента (рибофлавинкиназа и ФАД-синтаза) активируются гормонами щитовидной железы.
Флавиновые коферменты ФМН и ФАД необходимы для производства флавоферментов и играют ключевую роль в липидном и энергетическом обмене, участвуют в клеточном дыхании, производстве антител, метаболизме лекарств и ксенобиотиков и во многих других ферментативных и окислительно-восстановительных реакциях, протекающих в аэробных организмах. ФМН в качестве кофермента используют 16 % флавоферментов, а ФАД – 84 %; только 5 флавоферментов способны использовать оба кофермента.
Флавоферменты участвуют в метаболизме фолиевой кислоты, катализируют ряд реакций, протекающих в ходе биосинтеза стероидов и гормонов щитовидной железы, необходимы для синтеза других кофакторов, таких как кофермент А, коферменты Q, гем, пиридоксальфосфат. У растений флавокоферменты катализируют процессы фоторепарации димеров тимидина в повреждённой ДНК; у растений и грибов выполняют роль хромофоров в фоторецепторах синего цвета; получены данные об участии ФМН и ФАД в реакциях биолюминесценции и регуляции циркадных ритмов у растений.
Метаболизм рибофлавина у животных и у человека
В высоких концентрациях рибофлавин содержится в тканях с высокой метаболической активностью (например, печень). Рибофлавином богаты также яйца, молочные продукты, ферментированные напитки (пиво). В продуктах растительного происхождения рибофлавина меньше, чем в животной пище.
С едой в организм рибофлавин поступает в связанной форме. В кислой среде желудка нековалентные связи коферментных форм витамина с белками разрушаются и происходит дефосфорилирование ФАД и ФМН. Из проксимального отдела тонкого кишечника рибофлавин диффундирует в энтероциты, на скорость абсорбции влияют жёлчные кислоты. Рибофлавин также участвует в кишечно-печёночной рециркуляции жёлчных кислот.
В крови рибофлавин циркулирует в связанном с белками виде – с альбумином и в меньшей степени с иммуноглобулинами. Транспорт рибофлавина из клеток во внеклеточную жидкость, молоко, сперму, спинномозговую жидкость и жёлчь происходит при помощи мембранного белка-транспортёра ABCG2 из суперсемейства АТФ-связывающих кассетных переносчиков. У животных и человека рибофлавин, ФАД и ФМН не запасаются в тканях и выводятся из организма вместе с мочой, поэтому витамин В2 обычно не накапливается в токсичных концентрациях.
Рибофлавин как фотосенсибилизатор
Рибофлавин является эндогенным фотосенсибилизатором, т. к. в его состав входит изоаллоксазиновое кольцо. В зависимости от условий рибофлавин под действием синего и ультрафиолетового излучения переходит в возбуждённое триплетное состояние и способен вступать в фотодинамические реакции I типа, в ходе которых образуются свободные радикалы, или в реакции II типа с образованием синглетного кислорода. Способность рибофлавина к фотоактивации делает его перспективным средством для фотодинамической терапии рака и ряда других заболеваний.