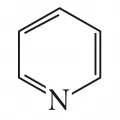
Пиридин
Пириди́н (1-азациклогекса-1,3,5-триен), шестичленное азотсодержащее гетероциклическое соединение.
Физико-химические свойства
Гигроскопичная бесцветная жидкость, с резким, неприятным запахом; смешивается с водой и спиртом во всех соотношениях, растворяется во многих органических растворителях, tкип 115,4 °C. Пиридин открыт шотландским химиком T. Андерсоном в 1849 г.; структура установлена немецким химиком В. Кёрнером в 1869 г. и, независимо от него, Дж. Дьюаром в 1871 г.
Пиридин – слабое основание, с неорганическими кислотами образует устойчивые соли, с алкилгалогенидами – соли N-алкилпиридиния, с галогенидами металлов, SO2, SO3, Br2, H2O – комплексные соединения. Пиридин проявляет химические свойства, характерные для третичных аминов (например, образует N-оксиды). Пиридин – ароматическое соединение. Электрофильное замещение протекает с большим трудом в мета-положение (большинство этих реакций протекает в кислой среде, в которой исходным соединением является не пиридин, а его соль). Пиридин нитруется лишь под действием NaNO3 или KNO3 в дымящей H2SO4 при 300 °C, образуя с небольшим выходом 3-нитропиридин; пиридин сульфируется олеумом в присутствии сульфата Hg при 220–270 °C до пиридин-3-сульфокислоты. Нуклеофильное замещение в пиридине протекает легче, чем в бензоле, и идёт по орто- и пара-положениям. Так, пиридин может реагировать с амидом натрия, образуя смесь орто- и пара-аминопиридинов (реакция Чичибабина). Пиридин, как правило, устойчив к окислителям, однако при действии надкислот образуется N-оксид пиридина. При 300 °C под действием FeCl3 пиридин окисляется в смесь изомерных дипиридилов общей формулы C5H4N−C5H4N. Каталитическое гидрирование в присутствии Pt или Ni, восстановление Na в спирте, а также электрохимическое восстановление приводит к пиперидину.
Получение
Пиридин содержится в каменноугольной смоле (около 0,08 % по массе пиридина), продуктах сухой перегонки древесины, торфа, костей. Пиридин выделяют главным образом из каменноугольной смолы, синтезируют из ацетилена и синильной кислоты HCN, из ацетальдегида и аммиака NH3 и т. д.
Биологическая роль
Пиридиновое кольцо играет важную роль в биологических процессах (в том числе с участием никотинамидадениндинуклеотида), является структурным фрагментом пиридиновых алкалоидов и т. д.
Применение
Пиридин и его производные применяют в синтезе красителей, лекарственных веществ, инсектицидов, в аналитической химии, как растворитель многих органических и некоторых неорганических веществ, для денатурации этилового спирта, в производстве винилпиридиновых каучуков и др. Комплексы пиридина используют в качестве сульфирующих, бромирующих реагентов и окислителей. Пиридин токсичен, действует на нервную систему, кожу.