Коферменты
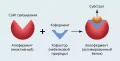
Коферме́нты [от лат. co(cum) – вместе и фермент] (коэнзимы), небольшие простые органические небелковые соединения, которые специфически связываются с апоферментами и образуют каталитически активный комплекс холофермент. Без коферментов апоферменты остаются неактивными; иногда коферменты и сами по себе проявляют слабые каталитические свойства, но взаимодействие апоферментов и коферментов даёт синергический эффект.
Большинство коферментов – это витамины или их метаболиты (например, фосфорилированные формы витаминов группы В). Так, производными тиамина (витамин В1) являются тиаминдифосфат (ТДФ), а также тиаминмонофосфат и тиаминтрифосфат; к производным рибофлавина (витамин В2) относятся флавинмононуклеотид (ФМН) и флавинадениндинуклеотид (ФАД); производные никотиновой кислоты (витамин РР) – это никотинамидадениндинуклеотид (НАД) и никотинамидадениндинуклеотидфосфат (НАДФ); производным пантотеновой кислоты (витамин В5) является кофермент А (КоА); к производным пиридоксина (витамин В6) относятся пиридоксальфосфат (ПФ) и пиридоксаминофосфат; производное фолиевой кислоты – тетрагидрофолат (ТГФ), и т. д. Нехватка витаминов в пище приводит к нарушениям обмена веществ.
Кофермент, который связывается с апоферментом при помощи прочных ковалентных связей и представляет собой неотъемлемую часть активного центра, называется простетической группой фермента (к ним относятся, например, ФАД и ФМН, биотин, гем).
Кофермент называется ко-субстратом в том случае, если он связывается с апоферментом, влияя на конформацию его активного центра; кофермент таким образом открывает возможность связывания фермента с субстратом. После завершения реакции ферментативного катализа такой кофермент высвобождается в изменённой форме и потом регенерируется в ходе отдельной, независимой реакции (например, НАД, НАДФ, КоА).
Некоторые коферменты связываются с аллостерическим центром фермента и являются аллостерическими эффекторами (активаторами или ингибиторами) (например, окисленная форма НАД+ и восстановленная форма НАДН).
Выделяют несколько основных групп коферментов.
Окислительно-восстановительные коферменты необходимы для переноса восстановительных эквивалентов – электронов, протонов и гидрид-ионов, при этом молекула субстрата окисляется, а молекула кофермента восстанавливается. В эту группу входят окисленные формы НАД+ и НАДФ+ (коферменты дегидрогеназ), ФМН и ФАД (коферменты дегидрогеназ, оксидаз и монооксигеназ), липоевая кислота (кофермент оксидоредуктаз), глутатион (кофермент глутатионпероксидазы), убихиноны (компоненты дыхательной цепи), гем (кофермент оксидоредуктаз, монооксигеназ и пероксидаз) и др.
Коферменты, задействованные в переносе групп, чаще всего входят в состав ферментов трансфераз. Так, КоА обеспечивает процесс переноса остатков ацильных групп в процессе синтеза и окисления жирных кислот, а также при окислении пирувата. Нуклеотиды, если они выступают в роли коферментов, переносят фосфатные группы в ходе гликолиза и других этапов углеводного обмена. ТДФ нужен для переноса гидроксиалкильных групп в транскетолазной реакции и в ходе декарбоксилирования кетокислот. ПФ участвует в реакциях трансаминирования и задействован в метаболизме аминокислот. Биотин в составе карбоксилаз обеспечивает транспорт активированной формы диоксида углерода. ТГФ способствует переносу С1-остатков в ходе синтеза пуриновых нуклеотидов, метионина и др. Кобаламид (аденозилкобаламин) является коферментом метилмалонил-КоА мутазы и задействован в реакции перестройки углеродного скелета.
Некоторые коферменты (например, КоА, АТФ, другие нуклеотиды) не только участвуют в переносе групп, но также необходимы для активации различных метаболитов или групп.