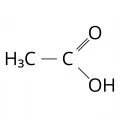
Уксусная кислота
У́ксусная кислота́ (этановая кислота, метанкарбоновая кислота), монокарбоновая кислота алифатического ряда, CH3СООН.
Историческая справка
Уксусная кислота в виде уксуса известна человеку с древнейших времён (6–5-е тыс. до н. э.). Способ получения ледяной уксусной кислоты разработал Т. Е. Ловиц в 1789 г. Из простейших неорганических веществ впервые синтезирована Г. Кольбе в 1845 г.
Физико-химические свойства
Бесцветная жидкость с резким запахом; молярная масса 60,052 г/моль. Безводная (ледяная) уксусная кислота представляет собой бесцветные или бледно-розовые кристаллы, обладает высокой гигроскопичностью; tпл 16,64 °C; tкип 117,9 °C; плотность 1,0491 г/см3 (при 20 °C). Смешивается во всех соотношениях с водой, диэтиловым эфиром, этанолом, бензолом и другими органическими растворителями, хорошо растворяет многие неорганические и органические вещества (например, серу, фосфор, ацетаты целлюлозы), не растворяется в сероуглероде. Образует двойные азеотропы с водой, тройные – с водой и бензолом (tкип 88 °C); кислота средней силы pKa 4,76 (25 °C).
По химическим свойствам – типичная карбоновая кислота. При хлорировании уксусной кислоты образуются моно-, ди- и трихлоруксусная кислоты. Восстановление уксусной кислоты алюмогидридом лития даёт этиловый спирт. Образует соли и эфиры (ацетаты), а также ангидрид, амид, галогенангидриды и др.
Раздражает слизистые оболочки верхних дыхательных путей и глаз, вызывает химические ожоги.
Нахождение в природе
В природе встречается в свободном виде или в виде солей и сложных эфиров в растениях (в зелёных листьях), в выделениях животных (моче, жёлчи), образуется при гниении и брожении (в кислом молоке, сыре, вине).
Получение
В промышленности уксусную кислоту преимущественно производят каталитическим карбонилированием метанола (катализаторы Rh, Co, Ir и др.). Пищевую уксусную кислоту получают уксуснокислым брожением этанола.
К менее распространённым методам получения относят жидкофазное окисление насыщенных углеводородов, например бутана, а также углеводородных фракций нефти (катализаторы Mn, Co и др.); окисление ацетальдегида (в присутствии солей Mn), этилена (катализатор Pd), этана (в присутствии Mo или V и др.); пиролиз древесины.
Объём мирового рынка уксусной кислоты в 2021 г. составил 16,7 млн т.
Применение
Уксусная кислота – сырьё в производстве винилацетата, ацетангидрида, ацетилхлорида, монохлоруксусной кислоты, ацетатов, а также многих красителей, инсектицидов, лекарств (аспирин, фенацетин). Как растворитель применяется в производстве терефталевой кислоты. В пищевой промышленности используют водные растворы пищевой уксусной кислоты (3–15%-ный – столовый уксус и 80%-ный – уксусная эссенция). Уксусная кислота – растворитель лаков, коагулянт латекса, ацетилирующий агент и реакционная среда в органическом синтезе.
Широкое применение находят производные уксусной кислоты. Соли уксусной кислоты используют при приготовлении пигментов (ацетаты Pb и Cu), как катализаторы (ацетаты Mn, Co, Zn) и протравы при крашении. Фенилуксусная кислота используется в парфюмерии и косметике.