Фотосинтез
Фотоси́нтез, процесс преобразования зелёными растениями и некоторыми бактериями энергии света в энергию химических связей органических соединений:
где H2A – восстановитель, который окисляется до A.
У высших растений, и цианобактерий восстановителем служит вода (H2O), а 2A – это кислород O2. В основе фотосинтеза лежат окислительно-восстановительные реакции, в ходе которых электроны переносятся от донора-восстановителя (H2O) к акцептору (CO2) с образованием восстановленных соединений (углеводы) и выделением молекулярного кислорода (O2). Такой фотосинтез называют оксигенным. Фотосинтезирующие бактерии, использующие в качестве донора-восстановителя не воду (H2O), а сероводород (H2S), аммиак (NH3), серу (S2), метан (CH4), молочную кислоту и другие легкоокисляемые соединения, O2 не выделяют.
Процесс фотосинтеза происходит в листьях, зелёных клетках стеблей, цветков, околоплодниках, черешках и даже в освещаемых корнях некоторых растений. Органеллой фотосинтеза является хлоропласт (у водорослей – хроматофор), который содержит различные пигменты – вещества, избирательно поглощающие свет в видимой части спектра.
Пигменты, участвующие в фотосинтезе высших растений, делятся на две группы: хлорофиллы (основные пигменты) и каротиноиды (вспомогательные пигменты). У пурпурных и зелёных бактерий, а также цианобактерий основными пигментами, участвующими в фотосинтезе, являются бактериохлорофиллы. У красных водорослей и цианобактерий роль вспомогательных ферментов выполняют фикобилины. У галобактерий фотосинтез осуществляется с помощью пигмент-белкового комплекса – бактериородопсина.
Развитие учения о фотосинтезе
В 1771 г. английский натуралист-любитель Дж. Пристли, проводя опыты с растениями, помещёнными в опрокинутый стеклянный кувшин, установил, что они способны «улучшать» воздух, «испорченный» при дыхании или горении свечи. В 1774 г. французским естествоиспытателем, основоположником современной химии А. Лавуазье, был получен молекулярный кислород.
В 1779 г. голландский врач Я. Ингенхауз показал, что зелёные растения выделяют O2 только на свету, однако при высоких температурах и интенсивности света они поглощают O2 и выделяют CO2.
В 1782 г. швейцарский естествоиспытатель Ж. Сенебье установил, что растения на свету не только выделяют O2, но и поглощают CO2. Процесс поглощения CO2 растениями Ж. Сенебье назвал «углеродным питанием». В 1800 г. им был издан трактат Physiologie végétale, в котором впервые предложен термин «физиология растений», а также определены задачи и методы новой науки.
В 1817 г. французские химики П. Пеллетье и Ж. Каванту выделили из листьев зелёное вещество и назвали его хлорофиллом. Важной ступенью в истории изучения фотосинтеза стало утверждение немецкого физика Р. Майера (1845) о том, что зелёные растения преобразуют энергию солнечного света в энергию химических соединений.
В 1865 г. немецкий учёный Ю. Сакс установил, что на свету в листьях образуется крахмал и он локализован в хлоропластах.
В 1871 г. российский естествоиспытатель К. А. Тимирязев, исследуя энергетику фотосинтеза, предположил, что хлорофилл способен к окислительно-восстановительному превращению. Позднее им была сформулирована идея о космической роли фотосинтеза как единственного процесса на Земле, благодаря которому солнечная энергия улавливается растением и трансформируется в энергию органических соединений (углеводов).
В 1881 г. немецкий физиолог Т. Энгельман экспериментально доказал, что кислород образуется в хлоропластах.
В 1893 г. российский биохимик А. Н. Бах предположил, что источником кислорода, образующегося при фотосинтезе, является вода.
Российский учёный М. С. Цвет в 1903 г. изобрёл новый метод разделения сложных веществ на компоненты – хроматографию, с помощью которой установил наличие двух модификаций хлорофилла: хлорофилл a и хлорофилл b, а также разделил жёлтые пигменты листа на три фракции.
В 1905 г. английский физиолог Ф. Блекман высказал предположение, что процесс фотосинтеза включает в себя световые реакции и не зависящие от света темновые реакции, для которых требуются вещества, образовавшиеся в световых реакциях.
Немецкий химик Р. Вильштеттер в 1906–1914 гг. определил элементарный состав хлорофиллов a и b. В 1915 г. за установление химического состава хлорофилла он был удостоен Нобелевской премии.
В 1914 г. один из основоположников отечественной физиологии растений, А. А. Рихтер, определил, что общая продолжительность акта фотосинтеза определяется темновой фазой. В 1920 г. немецкий биохимик О. Варбург доказал, что продолжительность световой фазы во много раз меньше темновой. В 1932 г. американскому учёному Р. Эмерсону удалось измерить продолжительность фаз фотосинтеза и показать, что скорость световых реакций во много раз выше темновых и они не зависят от температуры. Немецкий биохимик Х. Фишер в 1930–1940 гг. полностью расшифровал структурную формулу хлорофиллов a и b. В 1937 г. английский учёный Р. Хилл привёл биохимическое доказательство существования световой и темновой фаз фотосинтеза.
Прямые экспериментальные доказательства фотоокисления воды были получены советскими учёными А. П. Виноградовым и Р. В. Тейс в 1945 г. Они также показали, что при фотосинтезе кислород выделяется при разложении воды, а не углекислого газа.
В 1954 г. американский биохимик и физиолог растений Д. Арнон установил, что световая фаза фотосинтеза протекает в тилакоидах хлоропласта, а темновая – в строме. Он обнаружил, что освещение растворов хлоропластов в присутствии молекул аденозиндифосфата (АДФ) и фосфата приводит к образованию аденозинтрифосфата (АТФ). Этот процесс был назван фотосинтетическим фосфорилированием.
В 1956 г. группе американских учёных во главе с М. Калвином удалось раскрыть сущность темновых реакций фотосинтеза, за что им была присуждена Нобелевская премия (1961).
В 1957 г. Р. Эмерсон, изучая зависимость фотосинтеза от длины волны света, высказал идею о существовании двух фотосистем. В 1961–1966 гг. английский биохимик П. Митчелл предложил гипотезу, объясняющую сопряжение транспорта электронов с фосфорилированием, известную сейчас как «хемиосмотическая теория Митчелла», за которую он был удостоен Нобелевской премии (1978).
В 1966 г. австралийские исследователи М. Хетч и Ч. Слэк предложили законченную схему цикла темновых реакций у C₄-растений (C4-фотосинтез). В 1972 г. американский учёный Э. Толберт открыл фотодыхание.
Дальнейшее изучение процессов фотосинтеза показало, что свет активирует некоторые ферменты, катализирующие реакции темновой фазы. Кроме того, для многих ферментов темновой фазы была обнаружена зависимость от циркадных ритмов.
Существенные успехи, достигнутые мировой наукой за последние десятилетия, связаны с разработкой представлений о структурно-функциональной организации фотосинтетического аппарата, изучением молекулярных механизмов преобразования энергии, путей превращения углерода и др.
В настоящее время традиционное деление процесса фотосинтеза на две фазы – световую и темновую – часто заменяют на «первичные процессы фотосинтеза» и «восстановление CO2, NO3- и SO42-» соответственно.
Первичные процессы фотосинтеза (световая фаза фотосинтеза)
Структура и функции фотосистем
У растений и цианобактерий световая фаза фотосинтеза включает в себя фотофизический и фотохимический процессы, которые требуют энергии света и осуществляются в мембранах обоих типов тилакоидов, где локализованы фотосинтетические системы – фотосистема I (ФС I) и фотосистема II (ФС II), а также компоненты электронн-транспортной цепи (ЭТЦ) и АТФазный комплекс.
Фотосистемы связаны между собой, но различаются по составу белков, пигментов и оптическим (спектральным) свойствам входящих в них пигментов. ФС I локализована в тилакоидах стромы и гран, а ФС II – в тилакоидах гран.
Каждая фотосистема представляет собой пигмент-белковый комплекс, куда входят реакционный центр (РЦ), антенный, или светособирающий, комплекс (ССК) и переносчики электронов. У высших растений выделено два реакционных центра, которые включают ассоциированные с белком молекулы пигмента-ловушки П700 (ФС I) или П680 (ФС II), представляющие собой димеры (т. е. две молекулы) хлорофилла a с максимумом поглощения света в наиболее длинноволновой части солнечного спектра – 700 или 680 нм соответственно.
В реакционном центре находится всего 1 % фотосинтетических пигментов, которые непосредственно участвуют в преобразовании энергии. Остальные 99 % пигментов играют вспомогательную роль, образуя ССК, в которых связаны с белками.
Два ССК расположены в реакционном центре ФС I и ФС II и связывают только молекулы ß-каротина хлорофилла a; два других – внешние ССК – связывают хлорофиллы a, b и каротиноиды. Каждый ССК содержит несколько сотен молекул хлорофиллов и каротиноидов.
В ССК молекулы хлорофиллов и каротиноидов выполняют функцию пигментов-сборщиков. Они поглощают энергию кванта света и передают её в реакционный центр пигментам-ловушкам П680 или П700. Передача (миграция) энергии осуществляется по принципу индуктивного резонанса благодаря очень тесному расположению пигментов. Установлено, что в ССК пигменты строго ориентированы друг относительно друга и расстояние между ними не превышает 1,15 нм. Скорость передачи энергии между пигментами составляет 10-10–10-9 с. Миграция энергии происходит только в одном направлении, строго от каротиноидов к хлорофиллам b (эффективность передачи энергии составляет 40 %), от хлорофиллов b к хлорофиллам a (эффективность передачи энергии составляет 90 %) и, наконец, в РЦ к пигменту-ловушке П680 или П700. Таким образом, функция пигментов – сборщиков ССК состоит в поглощении энергии кванта света и её передаче реакционному центру, содержащему особые молекулы хлорофилла a – П700 или П680. На этом фотофизический процесс фотосинтеза заканчивается.
Поглотив энергию кванта света, электроны молекулы хлорофилла поднимаются на более высокий энергетический уровень, а сама молекула переходит в возбуждённое состояние. Приобретённый избыток энергии (т. н. энергия возбуждения) может быть перенесён на другую молекулу пигмента, растрачен в виде тепла, на испускание кванта света (флуоресценция, фосфоресценция) или использован в окислительно-восстановительной реакции (в фотохимическом процессе фотосинтеза).
В последнем случае в реакционном центре энергия возбуждения хлорофилла используется для первичного разделения зарядов, т. е. отщепления электронов от молекулы пигмента (она окисляется, становится заряженной положительно) и передачи их первичному акцептору, который восстанавливается (получает отрицательный заряд) и далее передаёт электроны переносчикам ЭТЦ. При оптимальном освещении разделение зарядов в РЦ происходит до 200 раз в секунду. Таким образом, в реакционном центре энергия возбуждённого состояния хлорофилла преобразуется в энергию разделённых зарядов, т. е. превращается в химическую энергию.
В ЭТЦ порядок расположения молекул-переносчиков зависит от их способности присоединять или отдавать электроны, т. е. величины окислительно-восстановительного потенциала (E'0).
Переносчиками электронов являются следующие белки: железосерные, или Fe-S-белки, ферредоксин, цитохромы b6 и f (образуют цитохромный b6f-комплекс), пластохиноны, флавиновые ферменты, пластоцианин, а также пиридиннуклеотиды (никотинамидадениндинуклеотидфосфат, НАДФ+).
Известны три пути транспорта электронов в ЭТЦ: нециклический, циклический и псевдоциклический.
Нециклический транспорт электронов
Нециклический транспорт электронов является основным в процессе фотосинтеза. В нём принимают участие две фотосистемы, которые осуществляют последовательный перенос электронов от ФС II к ФС I. В ФС II нециклический транспорт электронов отвечает за продукцию окислительного потенциала, необходимого для расщепления молекулы воды, в ФС I является сильным восстановителем и отвечает за образование богатого энергией кофермента – восстановленного НАДФН.
Диаграмма, на которой переносчики электронов расположены в соответствии со своим E'0, имеет форму буквы Z, поэтому получила название Z-схемы фотосинтеза.
 Электрон-транспортная цепь хлоропластов (Z-схема фотосинтеза).Молекула П700 (E'0 = +0,43 В) ФС I, поглотив квант света, переходит в возбуждённое состояние (П700*, E'0 = −0,8 В) и приобретает способность отдавать электроны первичному акцептору – мономерной форме хлорофилла a. Отдав электрон, молекула П700 окисляется и приобретает положительный заряд П700+. Далее электрон переходит через ряд переносчиков ЭТЦ (Fe-S-белки, ферредоксин), расположенных в порядке возрастания E'0, на конечный акцептор – НАДФ+, восстанавливая его до НАДФН. Источником электрона, заполняющего свободное место в П700+, является молекула П680 (E'0 = +1,18 В) ФС II. При поглощении энергии кванта света молекула П680 переходит в возбуждённое состояние (П680*, E'0 = −0,8 В) и приобретает способность отдавать электроны акцептору – феофитину (хлорофилл, в котором отсутствует магний). Феофитин выполняет роль промежуточного акцептора электрона между первичным донором П680 и первичным акцептором электрона, пластохиноном QA. Далее электрон, теряя энергию, переходит через ряд белков-переносчиков ЭТЦ к П700+.
Электрон-транспортная цепь хлоропластов (Z-схема фотосинтеза).Молекула П700 (E'0 = +0,43 В) ФС I, поглотив квант света, переходит в возбуждённое состояние (П700*, E'0 = −0,8 В) и приобретает способность отдавать электроны первичному акцептору – мономерной форме хлорофилла a. Отдав электрон, молекула П700 окисляется и приобретает положительный заряд П700+. Далее электрон переходит через ряд переносчиков ЭТЦ (Fe-S-белки, ферредоксин), расположенных в порядке возрастания E'0, на конечный акцептор – НАДФ+, восстанавливая его до НАДФН. Источником электрона, заполняющего свободное место в П700+, является молекула П680 (E'0 = +1,18 В) ФС II. При поглощении энергии кванта света молекула П680 переходит в возбуждённое состояние (П680*, E'0 = −0,8 В) и приобретает способность отдавать электроны акцептору – феофитину (хлорофилл, в котором отсутствует магний). Феофитин выполняет роль промежуточного акцептора электрона между первичным донором П680 и первичным акцептором электрона, пластохиноном QA. Далее электрон, теряя энергию, переходит через ряд белков-переносчиков ЭТЦ к П700+.
Таким образом, компоненты ЭТЦ соединяют между собой две фотосистемы. Цепь транспорта электронов включает следующие белки-переносчики: пластохиноны, цитохромный b6f-комплекс и пластоцианин. На участке транспорта электронов через цитохромный b6f-комплекс к П700+ возникает электрохимический градиент протонов за счёт переноса протонов из стромы через мембрану во внутритилакоидное пространство, который используется для образования АТФ из АДФ и неорганического фосфата (Фн).
Подробный механизм образования АТФ изложен в хемиосмотической теории (гипотезе), которую предложил П. Митчелл. Процесс преобразования энергии квантов света в энергию химических связей молекул АТФ был назван фотосинтетическим фосфорилированием (фотофосфорилирование), в отличие от окислительного фосфорилирования, наблюдаемого в митохондриях. В данном случае процесс образования АТФ из АДФ и неорганического фосфата (Фн) сопряжён с нециклическим транспортом электронов, поэтому получил название нециклического фотофосфорилирования.
Донором недостающего электрона для П680+ служат ионы марганца, образующие активный центр (Mn-кластер) водоокисляющего комплекса ФС II, в который входят также ионы хлора и кальция. В процессе последовательной передачи 4 электронов от водоокисляющего комплекса через промежуточный переносчик тирозин Z (остаток тирозина одного из белков ФС II) к П680+ происходит фотоокисление 2 молекул воды, которое сопровождается образованием 4 протонов (переносятся во внутритилакоидное пространство) и выделением в атмосферу молекулы кислорода:
Таким образом, при нециклическом транспорте электронов происходит перенос электронов от воды (E'0 = +0,81 В) к НАДФ+ (E'0 = −0,32 В). В процессе участвуют две фотосистемы, которые образуют единую систему переноса электронов. Продуктами нециклического транспорта электронов являются АТФ и НАДФН. Суммарное уравнение нециклического фотофосфорилирования следующее:
Циклический транспорт электронов с участием ФС I
Циклический транспорт электронов с участием ФС I является эволюционно самым древним. Он происходит тогда, когда соотношение между НАДФН и НАДФ+ достаточно велико.
Входящий в состав реакционного центра димер хлорофилла a П700 (E'0 = +0,43 В), поглотив квант света, переходит в возбуждённое состояние (П700*, E'0 = −0,8 В). Отдавая электрон акцептору, молекула П700 окисляется и приобретает положительный заряд П700+. Первичным акцептором электронов является мономерная форма хлорофилла a. От него электроны передаются по цепи переносчиков (Fe-S-белок, ферредоксин, пластохиноны, цитохромный b6f-комплекс, пластоцианин) с постепенной потерей энергии и возвращаются к П700+, который в данном случае выступает одновременно и донором, и акцептором электронов.
Одновременно с электронами пластохиноны транспортируют через тилакоидную мембрану протоны, что создаёт электрохимический градиент протонов. Выделяемая в ходе окислительно-восстановительных реакций энергия частично используется на образование АТФ (в частности, на участке ЭТЦ между цитохромами b и f). В данном случае процесс образования АТФ за счёт энергии света, сопряжённый с циклическим транспортом электронов, получил название циклического фотофосфорилирования. При циклическом транспорте электронов АТФ представляет собой единственный продукт световой фазы фотосинтеза. Циклическое фотофосфорилирование является дополнительным источником АТФ для восстановления CO2 в темновой фазе процесса фотосинтеза. Его активность повышается при нахождении растений в условиях абиотического стресса.
Циклический транспорт электронов с участием ФС II
Циклический транспорт электронов с участием ФС II представляет собой перенос электронов от восстановленных пластохинонов к П680+. Он является дополнительным источником АТФ и происходит, когда повреждён водоокисляющий комплекс (следовательно, кислород не выделяется) или наблюдается высокая интенсивность света. Предполагают, что этот процесс может протекать при закрытых устьицах, т. к. CO2 для него не нужен.
Псевдоциклический транспорт электронов
Процесс псевдоциклического транспорта электронов активируется в условиях дефицита НАДФ+ и при наличии высокой интенсивности света. В нём участвуют две фотосистемы и белки-переносчики ЭТЦ. При псевдоциклическом транспорте электроны переносятся от H2O на O2 с образованием супероксидрадикала (O2·-), одной из форм активированного кислорода, восстановление которого происходит в ФС I или ФС II, при этом синтезируется АТФ (псевдоциклическое фотофосфорилирование). Часто происходит так, что в ходе процесса единственным продуктом является АТФ, потому что потребление O2 компенсирует его образование при фотоокислении H2O.
Биохимическое значение первичных процессов фотосинтеза (световой фазы)
У высших растений первичные процессы фотосинтеза (световая фаза) обусловлены вызванным поглощённым светом транспортом электронов, в результате которого происходит фотоокисление воды (разрыв химических связей восстановителя) с выделением молекулярного кислорода и преобразование электромагнитной энергии в энергию химических связей АТФ и НАДФН – первичных стабильных продуктов, которые в дальнейшем используются при восстановлении CO2 и образовании конечных продуктов фотосинтеза.
Восстановление CO₂, NO₃- и SO₄²- (темновая фаза фотосинтеза)
Темновая фаза фотосинтеза включает в себя комплекс биохимических реакций восстановления атмосферного CO2, поступающего через межклетники листа в хлоропласты, а также восстановления корнем NO3- и SO42- – до органических соединений с использованием продуктов световой фазы. Известны различные пути восстановления CO2: C3-цикл (C3-фотосинтез, цикл Калвина, пентозофосфатный цикл), C4-цикл (C₄-фотосинтез, цикл Хетча – Слака – Карпилова), САМ-фотосинтез (от англ. Crassulacean Acid Metabolism, кислотный метаболизм толстянковых), фотодыхание (C2-фотосинтез, гликолатный цикл).
C₃-цикл восстановления CO₂
C3-цикл восстановления CO2 является основным у растений и происходит в ходе последовательных ферментативных превращений – цикла Калвина (назван по имени описавшего его М. Калвина).
Растения, у которых функционирует только C3-цикл, получили название C3-растений. Ферменты, осуществляющие фиксацию CO2 и его восстановление до сахаров, расположены в строме хлоропласта. Цикл Кальвина.
Цикл Кальвина.
В цикле Калвина выделяют четыре стадии:
1. Стадия карбоксилирования. На этой стадии происходит присоединение CO2 к 5-углеродному сахару – рибулозо-1,5-бифосфату (РуБФ). Реакцию карбоксилирования осуществляет фермент рибулозобифосфаткарбоксилаза – самый распространённый белок на Земле. Кроме карбоксилазной активности, этот фермент проявляет оксигеназную активность (присоединяет O2 в процессе фотодыхания). Поэтому полное название фермента – рибулозобифосфаткарбоксилазаоксигеназа (РуБисКО). Продукт реакции карбоксилирования – нестойкое 6-углеродное соединение, которое распадается на 2 молекулы 3-фосфоглицериновой кислоты (3-ФГК). Молекула 3-ФГК является первичным продуктом включения CO2 в органические вещества и содержит 3 атома углерода, поэтому этот способ фиксации CO2 называют C3-цикл.
2. Стадия восстановления ФГК. При участии АТФ и НАДФН – продуктов световой фазы, 3-ФГК восстанавливается до 2 молекул 3-фосфоглицеринового альдегида (3-ФГА). Молекулы 3-ФГА частично превращаются в изомер дигидроацетонфосфат (ДГАФ).
3. Стадия регенерации рибулозо-1,5-бифосфата (РуБФ). 3-ФГА взаимодействует с ДГАФ с образованием фруктозо-1,6-бифосфата, которая в ходе последующих реакций превращается в рибулозо-5-фосфат. При участии АТФ рибулозо-5-фосфат фосфорилируется до РуБФ – первичного акцептора CO2, что и обеспечивает непрерывную работу цикла. Если цикл проходит 3 раза, то во второй стадии образуется 6 молекул 3-ФГА, из которых 5 используются для регенерации 3 молекул РуБФ, а оставшаяся молекула выходит из цикла и включается в синтетические процессы.
4. Стадия синтеза углеводных продуктов фотосинтеза. При оптимальной интенсивности света триозы (3-ФГА, ДГАФ) используются в хлоропласте для образования первичного крахмала или транспортируются в цитозоль и участвуют в синтезе сахарозы, тогда как в условиях низкой освещённости участвуют в образовании органических кислот.
Среди первых продуктов фотосинтеза обнаружены аминокислоты. Из промежуточных продуктов цикла Калвина могут образовываться жиры и липиды. С учётом того что основным продуктом фотосинтеза являются углеводы (гексозы), цикл Калвина можно представить в виде следующего суммарного уравнения:
Поскольку в этом цикле (стадия регенерации РуБФ) образуются пентозы (например, рибулозо-5-фосфат, ксилулозо-5-фосфат), то его также называют пентозофосфатный цикл, или восстановительный пентозофосфатный цикл.
C₄-цикл восстановления CO₂
C4-фотосинтез (C4-цикл, C4-путь, цикл Хетча – Слака – Карпилова), комплекс биохимических 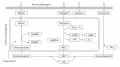 Реакции темновой фазы фотосинтеза, протекающие у С₄-растений в клетках мезофилла.реакций восстановления атмосферного углекислого газа (CO2), первыми продуктами которого являются органические кислоты (яблочная, щавелевоуксусная и аспарагиновая), содержащие 4 атома углерода.
Реакции темновой фазы фотосинтеза, протекающие у С₄-растений в клетках мезофилла.реакций восстановления атмосферного углекислого газа (CO2), первыми продуктами которого являются органические кислоты (яблочная, щавелевоуксусная и аспарагиновая), содержащие 4 атома углерода.
Эволюционно C4-фотосинтез возник позже, чем C3-фотосинтез, поэтому у древесных растений он не обнаружен. Растения, имеющие C4-фотосинтез, называются C4-растениями.
C4-растения характеризуются высокой фотосинтетической продуктивностью и имеют преимущества перед C3-растениями при дефиците воды в почве.
CAM-фотосинтез
CAM-фотосинтез, двухэтапный комплекс биохимических реакций, которые разделены во  Реакции темновой фазы фотосинтеза у САМ-растений.времени: в тёмное время суток происходит связывание и запасание атмосферного углекислого газа (CO2) в вакуолях клеток (в виде яблочной кислоты), а днём – его высвобождение и включение в цикл Калвина.
Реакции темновой фазы фотосинтеза у САМ-растений.времени: в тёмное время суток происходит связывание и запасание атмосферного углекислого газа (CO2) в вакуолях клеток (в виде яблочной кислоты), а днём – его высвобождение и включение в цикл Калвина.
CAM-метаболизм был впервые обнаружен у растений из семейства толстянковых (Crassulaceae). В настоящее время он описан у представителей 33 семейств. Растения, имеющие CAM-метаболизм, называют CAM-растениями.
Фотодыхание
Фотодыхание – активируемый светом процесс поглощения растениями O2 и выделения CO2. В присутствии высоких (около 2 %) концентраций O2 ключевой фермент C3-цикла РуБисКо функционирует как оксигеназа (присоединяет O2 к РуБФ).
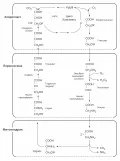 Фотодыхание.В ходе эволюции фотодыхание возникло как защита фотосинтетического аппарата растений от растущей концентрации атмосферного кислорода, выделяемого при фотосинтезе.
Фотодыхание.В ходе эволюции фотодыхание возникло как защита фотосинтетического аппарата растений от растущей концентрации атмосферного кислорода, выделяемого при фотосинтезе.
Фотодыхание осуществляется в результате взаимодействия трёх органелл – хлоропластов, пероксисом и митохондрий.
В процессе фотодыхания в хлоропластах и пероксисомах происходит поглощение O2, тогда как в митохондриях – выделение CO2.
Учитывая, что первичными продуктами фотодыхания являются фосфогликолат, гликолат и глиоксилат – двухуглеродные органические кислоты, этот процесс также называют C2-фотосинтезом, или гликолатным циклом. Фотодыхание является источником азотистых соединений – аминокислот глицина и серина.
Биологическое значение процесса фотосинтеза
Фотосинтез – единственный процесс в биосфере, ведущий к увеличению свободной энергии биосферы за счёт внешнего источника – Солнца и обеспечивающий существование как растений, так и всех гетеротрофных организмов, в том числе человека. Способность использовать солнечную энергию и вводить её в биосферные процессы и определяет космическую роль зелёных растений, о которой говорил и писал великий русский учёный К. А. Тимирязев.
Ежегодно в результате фотосинтеза на Земле образуется 160–200 млрд т органического вещества и выделяется 100–150 млрд т кислорода. Фотосинтетическое окисление воды является основным источником атмосферного кислорода. Кругооборот кислорода, углерода и других элементов, вовлекаемых в фотосинтез, создал и поддерживает современный состав атмосферы. Фотосинтез препятствует увеличению концентрации CO2 в атмосфере, предотвращая перегрев Земли вследствие парникового эффекта. Кислородно-озоновый экран атмосферы необходим для защиты от УФ-излучения.
Запасённая в продуктах фотосинтеза энергия (в виде различных видов топлива – торф, нефть, каменный уголь, древесина, природный газ) является основным источником энергии для человека. Однако запасы ископаемого топлива ограниченны на планете. Предполагается, что в энергетике будущего фотосинтез может занять одно из первых мест в качестве неиссякаемого и не загрязняющего среду источника энергии (создание «плантаций» быстрорастущих растений с последующим использованием растительной массы для получения тепловой энергии или переработки в высококачественное топливо).
Не менее важна роль фотосинтеза как основы получения продовольствия, кормов, технического сырья. Несмотря на высокую эффективность начальных стадий (около 95 %), в биомассу переходит менее 1–2 % солнечной энергии; потери обусловлены неполным поглощением света, лимитированием процесса на биохимическом и физиологическом уровнях.
Обеспечение растений водой, минеральным питанием, CO2, селекция сортов с высокой эффективностью фотосинтеза, создание благоприятной для светопоглощения структуры посевов и другие пути используются в целях реализации значительных резервов фотосинтетической продуктивности. Для ряда культур оправданны выращивание при полном или частичном искусственном освещении, биотехнологические способы получения растительной массы (особенно одноклеточных организмов), аквакультура для некоторых водорослей и т. д. В связи с этим особенно актуальными становятся разработка теоретических основ управления фотосинтезом, исследование фотосинтеза как целостного процесса, закономерностей его регулирования и адаптации к внешним условиям.
В 21 в. перед учёными стоит глобальная задача – выяснить молекулярные механизмы преобразования энергии в процессе фотосинтеза, что необходимо не только для развития фундаментальной науки, но и для создания новых нанобиотехнологий. В качестве альтернативного источника энергии активно проектируются системы искусственного фотосинтеза (например, солнечные ячейки на основе компонентов фотосинтетического аппарата), проводится поиск высокоэффективных катализаторов, осуществляющих процесс окисления воды. Разработка искусственных фотохимических систем, способных генерировать молекулярный водород (т. н. фотоводород) и кислород за счёт электронов и протонов от воды и энергии солнечного света, обеспечит население Земли экологически чистым видом топлива и энергии. Достигнутые в мире в этом направлении успехи позволяют считать искусственный фотосинтез реальностью ближайшего будущего.
