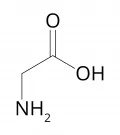
Глицин
Глици́н (гликокол, аминоуксусная кислота, аминоэтановая кислота), общепринятые сокращения: Gly, G, Гли, H2NCH2COOH, α-аминокислота простейшей структуры, содержащая в качестве боковой цепи только атом водорода. Не имеет оптических изомеров. Молярная масса 75,07 г/моль. Плотность 1,607 г/см3. Температура плавления 262 °C (с разложением). Впервые глицин был выделен А. Браконно при кислотном гидролизе желатина (выпаривании с серной кислотой) в 1820 г.
Глицин – протеиногенная α-аминокислота, кодируется триплетами, начинающимися с GG (GGU, GGC, GGA и GGG), присутствует во всех белках (частота встречаемости 7,04), входит в состав значительного числа биологически активных соединений, является предшественником многих клеточных метаболитов, выступает в роли нейромедиатора. Глицин является заменимой аминокислотой для человека и может быть синтезирован в организме.
Физико-химические свойства
Глицин – бесцветное кристаллическое вещество, хорошо растворимое в воде [25,3 г/100 мл (25 °C), 57,5 г/100 мл (75 °C)], умеренно растворимое в этиловом спирте [0,043 г/100 мл (25 °C)], малорастворимое в пиридине, ацетоне, нерастворимое в диэтиловом эфире.
Как и другие аминокислоты, в кристаллах и полярных растворителях глицин существует в виде цвиттер-иона. Его изоэлектрическая точка равна 5,97. Константы диссоциации кислоты (рКа) составляют 2,34 для карбоксильной группы (α-COOH) и 9,58 для аминогруппы (α-NH3+).
Глицин взаимодействует с кислотами и щелочами, образует комплексы с металлами, вступает в реакции, характерные для карбоновых кислот и аминов, а именно: реакции этерификации, взаимодействие с аминами, декарбоксилирование, реакции с азотистой кислотой, окислительное дезаминирование, переаминирование, N-алкилирование, N-ацилирование, образование пептидной связи.
Способы получения
Химически глицин можно получить в ходе хлорирования уксусной кислоты и дальнейшего взаимодействия продукта реакции с аммиаком, через аммонолиз и последующее окисление водных растворов гликолонитрила или щелочным гидролизом гидантоина. В промышленной практике наиболее распространен способ получения глицина аммонолизом монохлоруксусной кислоты в водный раствор в присутствии гексаметилентетрамина.
Участие в обмене веществ
Предшественником в биосинтезе глицина служит 3-фосфоглицерат (сложный эфир глицериновой и ортофосфорной кислот). Глицин может быть синтезирован из серина под действием ферментов серингидроксиметилтрансферазы (КФ 2.1.2.1) и глицинсинтазы [КФ 2.1.2.10 + КФ 1.4.4.2 (+ КФ 1.8.1.4)]. Кроме того, возможен биосинтез глицина из холина, гидроксипролина или треонина. Катаболизм глицина происходит за счёт обратных реакций синтеза, а также под действием оксидазы D-аминокислот.
Глицин – гликогенная аминокислота, продуктом метаболизма глицина является пируват. Глицин служит предшественником при биосинтезе креатина, участвующего в энергетическом обмене в клетках мышц и мозга, пуриновых оснований, входящих в состав ДНК, РНК, коферментов, алкалоидов, токсинов и порфириновых соединений (гем, хлорофилл).
Глицин – тормозной нейромедиатор ряда клеток спинного мозга и стволовых структур головного мозга взрослых особей человека и других позвоночных. В мозге эмбриона является возбуждающим нейромедиатором. Переключение глициновой системы с функции возбуждения на функцию торможения после рождения происходит постепенно «от хвоста к голове». У крыс, например, этот процесс завершается на 16-й день, для человека подобных данных пока нет. Глицин также необходим для активации глутаматных рецепторов за счет связывания со специальным модуляторным участком.
Глицин входит в состав консенсусных последовательностей многих белков, например киназ, натриевых и калиевых каналов, где за счёт малого размера боковой цепи он обеспечивает гибкость полипептидной цепи.
Особенно богаты глицином склеропротеины: например, в фиброине шёлка 43,6% аминокислотных остатков приходится на долю глицина. Структура фиброина состоит из повторяющейся аминокислотной последовательности (Gly-Ser-Gly-Ala-Gly-Ala)n, которая формирует антипараллельные складчатые β-слои, связанные водородными связями. Около 30% аминокислотных остатков приходится на долю глицина в коллагене. Глицин, наряду с расположенным рядом пролином или гидроксипролином, стабилизирует спирали коллагена за счет тесного контакта коллагеновых фибрилл в молекуле, позволяющего образование водородных связей и межмолекулярных сшивок. Среди антимикробных пептидов беспозвоночных выделяют глицин-богатые (акалолептины, акантоскуррин и др.).
Глицин входит в состав множества биологически активных соединений, например глутатиона, важнейшего клеточного антиоксиданта, гликохолевой кислоты, необходимой для переваривания жиров, гиппуровой кислоты, продукта связывания токсичной бензойной кислоты.
Наследственное нарушение метаболизма глицина может приводить к накоплению в почках и мочевыводящих путях солей щавелевой кислоты (оксалоз), повышенному выделению глицина с мочой (глицинурия) или повышению его содержания в крови (глицинемия).
Применение
Глицин применяется в медицине в качестве ноотропного средства. Бетаин глицина (внутрисолевая форма триметилглицина) – компонент соков растений, используют в качестве лекарственного средства, пищевой добавки. Производное глицина 4-гидроксифениламиноуксусная кислота (также называемое «глицин») применяется как проявитель в фотографии. Глицин и его натриевая соль – пищевая добавка Е640, модификатор вкуса и аромата.