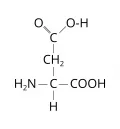
Аспарагиновая кислота
Аспараги́новая кислота́ (α-аминоянтарная кислота, 2-аминобутадионовая кислота, общепринятые сокращения Asp, D, Асп), HOOCCH2CH(NH2)COOH, моноаминодикарбоновая, кислая гидрофильная α-аминокислота. Содержит асимметрический атом углерода, обладает оптической активностью, существует в виде двух энантиомеров – L-аспарагиновая кислота и D-аспарагиновая кислота. В природе преобладает L-форма аспарагиновой кислоты. Молярная масса 133,12 г/моль. Плотность 1,66 г/см3. Температура плавления 270 °C (с разложением). Впервые аспарагиновая кислота была выделена в 1868 г. К. Г. Риттхаузеном из бобовых.
L-аспарагиновая кислота – протеиногенная аминокислота, кодируется триплетами, начинающимися с GA (GAU, GAC), присутствует во всех белках (частота встречаемости 5,49), входит в состав значительного числа биологически активных соединений, широко распространена в органах и тканях различных организмов в свободном состоянии, а также в виде амида (аспарагин) и других производных, служит предшественником для многих клеточных метаболитов. L-аспарагиновая кислота является заменимой для человека аминокислотой (может быть синтезирована в организме).
Физико-химические свойства
Аспарагиновая кислота – бесцветное кристаллическое вещество, растворимое в горячей воде [6,9 г/100 мл (100 °C)], разбавленной соляной кислоте, малорастворимое в холодной воде [0,5 г/100 мл (25 °C)], нерастворимое в этаноле, диэтиловом эфире, бензоле, пиридине.
Как и другие аминокислоты, в кристаллах и полярных растворителях аспарагиновая кислота существует в виде цвиттер-иона. Её изоэлектрическая точка равна 2,77. Константы диссоциации кислоты (рКа) составляют 1,88 для карбоксильной группы (α-COOH), 3,65 (β-COOH) и 9,60 для аминогруппы (α-NH3+).
Аспарагиновая кислота взаимодействует с кислотами и щелочами, образует комплексы с металлами, вступает в реакции, характерные для карбоновых кислот и аминов, а именно: реакции этерификации, взаимодействие с аминами, декарбоксилирование, реакции с азотистой кислотой, окислительное деаминирование, переаминирование, N-алкилирование, N-ацилирование, образование пептидной связи.
Способы получения
Химико-ферментативный метод позволяет получить L-аспарагиновую кислоту из фумарата аммония под действием аспартазы (КФ 4.3.1.1).
Участие в обмене веществ
Биосинтез L-аспарагиновой кислоты происходит за счёт реакции трансаминирования с участием щавелевоуксусной и L-глутаминовой кислот. L-аспарагиновая кислота – гликогенная аминокислота, конечным продуктом её катаболизма является оксалоацетат. L-аспарагиновая кислота служит предшественником в синтезе L-аспарагина, L-метионина, L-треонина и L-лизина, а также никотиновой кислоты при их биосинтезе у растений и микроорганизмов.
L-аспарагиновая кислота играет важную роль в азотистом обмене: участвует в синтезе пиримидиновых оснований, мочевины, в реакциях переаминирования, связывает и переносит аммиак.
L-аспартат – участник малат-аспартатной челночной системы для переноса восстанавливающих эквивалентов от цитозольного никотинамидадениндинуклеотида в митохондриальный матрикс.
L-аспарагиновая кислота входит в состав молекул белков (кроме протаминов) (12 % в эдестине, 10,3 % в глобулине ячменя).
Остаток L-аспарагиновой кислоты часто присутствует в активном сайте ферментов [например, аспарагиновых эндопептидаз (КФ 3.4.23), сериновых протеаз/сериновых эндопептидаз (КФ 3.4.21), гликозил-гидролаз (3.2.1), пирофосфатаз (КФ 3.6.1), нуклеаз (КФ 3.1)].
L-аспарагиновая кислота подвержена спонтанной рацемизации (обращению конфигурации) in vivo. Для человека за год соотношение D-Asp/L-Asp в дентине увеличивается на 0,12 % в молочных и 0,06 % в постоянных зубах, в эластине от 0,11 % до 0,41 % в зависимости от вида ткани. С возрастом накопление остатков D-аспарагиновой кислоты в белках нарушает их функцию и приводит к развитию заболеваний [например, катаракты (белки кристаллины), сердечно-сосудистых заболеваний (белок эластин)]. Свободная D-аспарагиновая кислота в организме человека и других млекопитающих участвует в нейрогенезе и эндокринной модуляции.
Применение
L-аспарагиновая кислота применяется в медицине в составе средств парентерального питания и ноотропных средств. Её используют для получения биосовместимого и биоразлагаемого полимера. Входит в состав аспартама (L-аспартил-L-фенилаланина) – подсластителя, заменителя сахара, пищевой добавки E951.