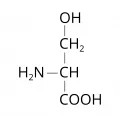
Серин
Сери́н (α-амино-β-гидроксипропионовая кислота, 2-амино-3-гидроксипропановая кислота, общепринятые сокращения: Ser, S, Сер), алифатическая гидроксиаминокислота, HOCH2CH(NH2)COOH. Содержит асимметрический атом углерода, обладает оптической активностью, существует в виде двух энантиомеров – L-серин и D-серин. В живой природе серин преимущественно встречается в L-конфигурации. Молярная масса 105,1 г/моль. Плотность 1,537 г/см3. Температура плавления 228 °C (с разложением). Впервые серин был получен из шёлкового клея в 1865 г. Э. Крамером.
L-серин – протеиногенная аминокислота, кодируется триплетами UCU, UCC, UCA, UCG, AGU и AGC, присутствует во всех белках (частота встречаемости 7,33), участвует в биосинтезе ряда аминокислот и многих биологически активных соединений, входит в состав активного центра ферментов, принимает участие в регуляции их активности.
L-серин может синтезироваться в организме человека и относится к заменимым аминокислотам.
Физико-химические свойства
Серин – бесцветное кристаллическое вещество, растворимое в воде [(для DL-серина 5,02 г/100 мл (25 °C), 19,21 г/100 мл (75 °C)], в 75%-ном этиловом спирте (0,187 г/100 мл), нерастворимое в абсолютном этаноле, диэтиловом эфире, бензоле, уксусной кислоте.
Как и другие аминокислоты, в кристаллах и полярных растворителях серин существует в виде цвиттер-иона. Его изоэлектрическая точка равна 5,68. Константы диссоциации кислоты (рКа) составляют 2,21 для карбоксильной группы (α-COOH) и 9,15 для аминогруппы (α-NH3+).
Серин взаимодействует с кислотами и щелочами, образует комплексы с металлами, вступает в реакции, характерные для карбоновых кислот и аминов, а именно: реакции этерификации, взаимодействие с аминами, декарбоксилирование, реакции с азотистой кислотой, окислительное деаминирование, переаминирование, N-алкилирование, N-ацилирование, образование пептидной связи. Характерными для серина являются реакции элиминирования, О-ацилирования.
Способы получения
L-серин получают химико-ферментативным методом из глицина, метанола при помощи фермента сериндегидраза (КФ 4.2.1.13).
Участие в обмене веществ
Предшественником в биосинтезе L-серина служит 3-фосфоглицерат (сложный эфир глицериновой и ортофосфорной кислот). L-серин – глюкогенная аминокислота, конечным продуктом его деградации в клетке является пируват.
Избыточная активация биосинтеза L-серина/L-глицина приводит к онкогенезу.
L-серин участвует в биосинтезе L-глицина, L-метионина, L-цистеина и L-триптофана, а также этаноламина, сфинголипидов, холина и др. Производные серина – антибиотики циклосерин и азасерин.
L-серин входит в состав активного центра ряда ферментов, в том числе протеаз (сериновые протеазы), гидролаз, фосфорилаз, щелочной фосфатазы.
Остаток L-серина служит точкой присоединения гликозоаминогликана к сердцевинному белку при образовании протеогликанов.
Фосфорилирование/дефосфорилирование L-серина регулирует активность многих ферментов, например для активации гликогенфосфорилазы (КФ 2.4.1.1) – фермента, который катализирует лимитирующую стадию процесса гликогенолиза, – необходимо фосфорилирование остатка Сер14. Работа многих клеточных рецепторов регулируется за счёт фосфорилирования/дефосфорилирования остатков L-серина.
Почти все белки содержат L-изомер серина; особенно богаты им белки шёлка – фиброин (до 16,2 % остатков) и серицин (до 40 %), трипсиноген (до 16,7 %), пепсин (до 12,2 %).
D-серин, образовавшийся под действием сериновой рацемазы из L-серина в астроцитах, поступает в нейроны и участвует в активации глутаматных рецепторов за счёт связывания со специальным модуляторным участком. Повышение уровня D-серина в плазме крови и ликворе наблюдают у пациентов при болезни Альцгеймера. D-серин накапливается в хрусталике глаза при старении человека и при развитии катаракты. Ростом уровня D-серина в крови сопровождаются заболевания почек из-за ухудшения его выделения.
D-серин содержится в пептидных антибиотиках (бацилломицине D, полимиксинах D1 и D2).
Применение
L-серин применяется в медицине в составе средств парентерального питания и ноотропных средств. DL-серин входит в состав антианемического препарата.