Соли (в химии)
Со́ли, класс химических соединений. Согласно теории электролитической диссоциации, соли – это вещества, полностью или частично диссоциирующие в водном растворе на катионы 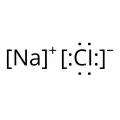 Структурная формула хлорида натрия.основания и анионы кислотного остатка. Являются продуктами замещения атомов H кислоты на металл или групп OH основания на кислотный остаток; при полном замещении образуются средние, или нормальные, соли, например хлорид натрия NaCl; при неполном замещении атомов H – кислые соли, например гидросульфат аммония NH4HSO4; при неполном замещении групп OH – оснóвные соли, например дигидроксостеарат алюминия (C17H35COO)Al(OH)2. Различают соли простые, включающие по одному виду катионов и анионов (например, карбонат калия K2CO3), двойные, содержащие два вида катионов (KCl·MgCl2), смешанные, в составе которых два вида кислотных остатков (AgClBr). Комплексные соли содержат комплексные ионы, например гексацианоферрат(II) калия K4[Fe(CN)6]. Внутренние соли представляют собой биполярные ионы, например бетаин глицина (CH3)3N+CH2COO–.
Структурная формула хлорида натрия.основания и анионы кислотного остатка. Являются продуктами замещения атомов H кислоты на металл или групп OH основания на кислотный остаток; при полном замещении образуются средние, или нормальные, соли, например хлорид натрия NaCl; при неполном замещении атомов H – кислые соли, например гидросульфат аммония NH4HSO4; при неполном замещении групп OH – оснóвные соли, например дигидроксостеарат алюминия (C17H35COO)Al(OH)2. Различают соли простые, включающие по одному виду катионов и анионов (например, карбонат калия K2CO3), двойные, содержащие два вида катионов (KCl·MgCl2), смешанные, в составе которых два вида кислотных остатков (AgClBr). Комплексные соли содержат комплексные ионы, например гексацианоферрат(II) калия K4[Fe(CN)6]. Внутренние соли представляют собой биполярные ионы, например бетаин глицина (CH3)3N+CH2COO–.
 Гексацианоферрат(II) калия.К солям относятся галогениды, неорганические сульфаты, нитраты, карбонаты, бораты, фосфаты и др. Большинство солей имеет ионную кристаллическую структуру, характеризуется относительно высокими температурами плавления и кипения. Различают соли хорошо растворимые в воде, малорастворимые и практически нерастворимые. Получают взаимодействием кислот с основаниями (реакция нейтрализации) или оснóвными оксидами; элементов с сильными кислотами или основаниями; реакциями обмена. Соли применяются в пищевой, металлургической, стекольной, кожевенной, текстильной отраслях промышленности, в сельском хозяйстве, в медицине и др.
Гексацианоферрат(II) калия.К солям относятся галогениды, неорганические сульфаты, нитраты, карбонаты, бораты, фосфаты и др. Большинство солей имеет ионную кристаллическую структуру, характеризуется относительно высокими температурами плавления и кипения. Различают соли хорошо растворимые в воде, малорастворимые и практически нерастворимые. Получают взаимодействием кислот с основаниями (реакция нейтрализации) или оснóвными оксидами; элементов с сильными кислотами или основаниями; реакциями обмена. Соли применяются в пищевой, металлургической, стекольной, кожевенной, текстильной отраслях промышленности, в сельском хозяйстве, в медицине и др.
