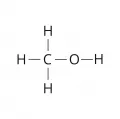
Метиловый спирт
Мети́ловый спирт (метанол, карбинол, древесный спирт), простейший представитель одноатомных алифатических спиртов, CH3OH.
Физико-химические свойства
Бесцветная жидкость с характерным алкогольным запахом; tкип 64,96 °C, плотность 791,4 кг/м3; смешивается в любых соотношениях с водой, спиртами, бензолом, ацетоном и другими органическими растворителями, не смешивается с алифатическими углеводородами; образует азеотропные смеси с ацетоном, бензолом, четырёххлористым углеродом и др.; легко воспламеняется и горит несветящимся, бледно-голубым пламенем. Метиловый спирт образует взрывоопасные смеси с воздухом (концентрационные пределы взрываемости 6,7–36,5 % CH3OH; температура вспышки 15,6 °C).
Метиловый спирт, как и другие первичные одноатомные спирты, проявляет амфотерные свойства (pKa 15,1). При действии щелочных металлов образуются метилаты (например, метилат натрия CH3ONá, при действии органических и неорганических кислот – сложные эфиры (например, с серной кислотой – метилсульфат CH3OSO2OH, с карбоновыми кислотами – метилалканоаты состава RCOOCH3. Каталитическое взаимодействие CH3OH с оксидом углерода CO приводит к образованию уксусной кислоты, со смесью CO и водорода H2 – этанола и других спиртов, аммиаком NH3 и анилином (в присутствии дегидратирующих катализаторов) – метиламинов и N,N-диметиланилина соответственно, с бензолом – толуола. Метиловый спирт разлагается водяным паром в присутствии катализатора на CO2 и H2 (по этой реакции получают водород 98%-ной чистоты в передвижных установках небольшой мощности). В результате высокотемпературной реакции над оксидом алюминия Al2O3 превращается в диметиловый эфир и над высококремнистыми цеолитами – в парафиновые и ароматические углеводороды. При неполном каталитическом окислении метилового спирта кислородом воздуха при 500–600 °С образуется формальдегид, формальдегид получается также при дегидрировании CH3OH.
Нахождение в природе
В природе метиловый спирт в свободном виде встречается редко (содержится в некоторых растениях, например в борщевике), больше распространены его эфиры.
Получение
Длительное время метиловый спирт вместе с ацетоном и уксусной кислотой получали при сухой перегонке древесины, однако в связи с созданием многотоннажного производства метилового спирта синтетическим путём способ утратил своё значение. Метиловый спирт производят главным образом на основе синтез-газа (процесс осуществляют при нагревании до 250–300 °С и давлении 6 МПа, в присутствии катализатора – оксидов меди и хрома); в качестве сырья для получения синтез-газа используют природный, попутный, коксовый и другие углеводородсодержащие газы (например, образующиеся при нефтепереработке).
Применение
Метиловый спирт применяют в основном для производства формальдегида, метиламинов, уксусной кислоты, метиловых эфиров карбоновых кислот (муравьиной, метакриловой, терефталевой и др.) и других продуктов многотоннажного нефтехимического производства, а также как метилирующий реагент в органическом синтезе; как растворитель и добавку к моторным топливам, повышающую их октановое число; как альтернативное моторное топливо.
Токсичность
Токсичен, действует преимущественно на нервную и сосудистую системы, обладает резко выраженным кумулятивным эффектом. При приёме внутрь смертельная доза для человека 30 мл, в количестве 5–10 мл вызывает тяжёлое отравление. Как при острых, так и при хронических отравлениях метиловым спиртом типичны поражения зрительного нерва и сетчатки глаза.