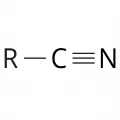Нитрилы карбоновых кислот
Нитри́лы карбо́новых кисло́т, производные карбоновых кислот общей формулы R−C≡N (R – органический радикал); часто рассматриваются как продукты замещения атомов водорода в молекуле циановодорода на органический радикал R – органические цианиды. Нитрилы – структурные изомеры изонитрилов. Могут содержать одну или несколько цианогрупп −C≡N, например ацетонитрил (нитрил уксусной кислоты) СН3−CN, азо-бис-изобутиронитрил NC(CH3)2CN=NC(CH3)2CN (динитрил азоизомасляной кислоты); помимо цианогрупп – другие функциональные группы, например гидроксильную (гидроксинитрилы). Впервые получены Ж.-Б. Дюма в 1847 г.
Низшие алифатические нитрилы – жидкости, высшие – твёрдые кристаллические вещества; простейший ароматический нитрил бензонитрил С6H5CN – бесцветная жидкость с запахом горького миндаля. Нитрилы плохо растворяются в воде (за исключением низших алифатических), хорошо смешиваются со многими органическими растворителями. Нитрилы образуют комплексы с солями металлов с участием неподелённой пары электронов атома азота или за счёт координации π-электронной системы цианогруппы к металлоцентру; восстанавливаются водородом в присутствии катализаторов до первичных аминов RCH2NH2; гидролизуются под действием кислот или растворов щелочей до карбоновых кислот RCOOH; реагируют с алкенами и их функциональными производными в присутствии кислотных катализаторов, образуя замещённые амиды; взаимодействуют с диеновыми углеводородами, давая алкилпиридины (диеновый синтез); восстанавливаются дихлоридом олова до альдегидов (реакция Стефена). При гидратации нитрилов в щелочной среде образуются амиды RCONH2. Нитрилы с ненасыщенными углеводородными остатками легко полимеризуются; например, в промышленности полимеризацией акрилонитрила получают полиакрилонитрильные волокна.
Основным методом получения нитрилов является дегидратация амидов RCONH2, аммониевых солей карбоновых кислот RCOONH4 или альдоксимов RCH=NOH при нагревании с оксидом фосфора(V), хлоридом фосфора(V), трихлороксидом фосфора(V) или тионилхлоридом. Нитрилы получают также алкилированием галогеналканами цианида калия, присоединением синильной кислоты по кратным связям, окислительным аммонолизом углеводородов и другими способами. Применяют нитрилы в качестве растворителей, инициаторов полимеризации, как сырьё в производстве волокнообразующих полимеров и смол, пластификаторов, лекарственных веществ, моющих средств, витаминов, пестицидов, красителей и др.
Токсичность нитрилов зависит от их строения (высокотоксичны, например, α-аминонитрилы и α-гидроксинитрилы) и обусловлена образованием в процессе метаболизма иона CN–, который блокирует многие ферменты, в том числе цитохромоксидазу (в результате теряется способность тканей усваивать кислород, что ведёт к развитию гипоксии). Отравление нитрилами может произойти при вдыхании паров, при попадании в желудочно-кишечный тракт, при проникновении через кожу.