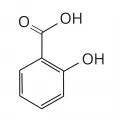
Салициловая кислота
Салици́ловая кислота́ (2-гидроксибензойная кислота, орто-оксибензойная кислота, о-карбоксифенол), простейшая ароматическая гидроксикислота, фенолокислота, HOC6H4COOH.  Ива.
Фото: Николай Потанин, flickr.com. CC BY-SA 2.0Соли и эфиры называются салицилатами. В природе встречается в растениях (в основном в виде гликозида метилсалицилата). Впервые выделена из коры ивы итальянским химиком Р. Пириа в 1938 г. Молярная масса 138,12 г/моль. Плотность 1,443 г/см3. tпл 159 °C. Начинает возгоняться при 76 °C.
Ива.
Фото: Николай Потанин, flickr.com. CC BY-SA 2.0Соли и эфиры называются салицилатами. В природе встречается в растениях (в основном в виде гликозида метилсалицилата). Впервые выделена из коры ивы итальянским химиком Р. Пириа в 1938 г. Молярная масса 138,12 г/моль. Плотность 1,443 г/см3. tпл 159 °C. Начинает возгоняться при 76 °C.
Физико-химические свойства
Салициловая кислота – бесцветное кристаллическое вещество,
 Образец салициловой кислоты.растворимое в этаноле [39,2 г/100 мл (15 °C)], диэтиловом эфире [50,5 г/100 мл (15 °C)], хлороформе, горячем бензоле, ацетоне, малорастворимое в воде [0,08 г/100 мл (0 °C), 0,18 г/100 мл (20 °C), 0,82 г/100 мл (60 °C), 1,76 г/100 мл (75 °C)], сероуглероде.
Образец салициловой кислоты.растворимое в этаноле [39,2 г/100 мл (15 °C)], диэтиловом эфире [50,5 г/100 мл (15 °C)], хлороформе, горячем бензоле, ацетоне, малорастворимое в воде [0,08 г/100 мл (0 °C), 0,18 г/100 мл (20 °C), 0,82 г/100 мл (60 °C), 1,76 г/100 мл (75 °C)], сероуглероде.
Показатели констант кислотности (pKa) составляют 2,9 и 13,1.
Салициловая кислота обладает химическими свойствами фенолов и ароматических карбоновых кислот. Электрофильное замещение проходит в орто- и пара-положения по отношению к гидроксильной группе и часто сопровождается декарбоксилированием. Так, при нитровании образуется 2,4,6-тринитрофенол (пикриновая кислота), при бромировании – 2,4,6-трибромфенол. При сульфировании салициловой кислоты олеумом декарбоксилирование не происходит и образуется 2-гидрокси-5-сульфобензойная кислота.
Салициловая кислота образует соли, сложные эфиры двух видов – по карбоксильной (COOH) и гидроксильной (OH) группам. Взаимодействует с анилином в присутствии хлорида фосфора(III) с образованием салициланилида.
При быстром нагревании выше 160 °C салициловая кислота декарбоксилируется до фенола. Нагревание в атмосфере диоксида углерода при 230 °C приводит к образованию фенилсалицилата. Медленное нагревание до 250 °C сопровождается циклизацией в 9-ксантенон.
Способы получения
В промышленности салициловую кислоту получают карбоксилированием фенолята натрия по реакции Кольбе – Шмитта.
Участие в обмене веществ
Салициловая кислота – важный метаболит растений, участвующий в регуляции роста, ответе на стресс, защите от патогенов. Она синтезируется из хоризмата по двум метаболическим путям, через промежуточное образование изохоризмата или фенилаланина. Салициловая кислота в растениях встречается в активной форме в виде свободной кислоты либо запасается в составе гликозидов и эфиров.
При попадании в организм человека бо́льшая часть салициловой кислоты конъюгирует с глицином и экскретируется с мочой в виде салицилуровой кислоты.
Применение
Салициловую кислоту применяют в медицине, косметологии. Как антисептик, она входит в состав препаратов для лечения кожных заболеваний (паста Лассара, мозольная жидкость и др.). Салициловая кислота и её производные (например, ацетилсалициловая кислота – аспирин) обладают жаропонижающим, противовоспалительным и болеутоляющим действием. Применяют при синтезе красителей, фунгицидов, душистых веществ.
Мировое производство салициловой кислоты в 2017 г. оценивается в 102,815 тыс. т. Ожидаемый ежегодный прирост производства до 2030 г. составляет 10 % (Salicylic acid market ... 2019).