Сульфирование
Сульфи́рование (сульфонирование), введение сульфогруппы (–SO2OH) в молекулу органического соединения; в широком смысле сульфирование – введение группы –SO2X (X = ОН, ONa, OAlk, OAr, Hal, NAlk2 и др.).
Процесс, обратный сульфированию (удаление группы –SO2X из молекулы органического соединения), называется десульфированием (десульфонированием).
Сульфирование осуществляют прямым путём с использованием сульфирующих агентов либо косвенным путём, например введением сульфогруппы в составе сульфоалкильных фрагментов (СН2)nSО2Х. Сульфирующие агенты: H2SO4, SO3 и его комплексы с органическими соединениями (эфирами, третичными аминами и фосфинами, амидами карбоновых кислот, три-алкилфосфатами и др.), олеум, SOCl2, галогенсульфоновые и сульфаминовые кислоты, диалкилсульфаты, ацил-сульфаты.
Сульфирование ароматических углеводородов протекает по механизму электрофильного замещения.
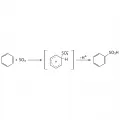 Механизм сульфирования ароматических углеводородов.Реакцию осуществляют как в паровой, так и в жидкой фазе (растворители: SO2, ССl4, хладоны и т. п.). При сульфировании серной кислотой для смещения равновесия вправо применяют избыток кислоты или связывают воду добавлением олеума, азеотропной отгонкой.
Механизм сульфирования ароматических углеводородов.Реакцию осуществляют как в паровой, так и в жидкой фазе (растворители: SO2, ССl4, хладоны и т. п.). При сульфировании серной кислотой для смещения равновесия вправо применяют избыток кислоты или связывают воду добавлением олеума, азеотропной отгонкой.
Соединение с электронодонорными заместителями более реакционноспособны и сульфируются преимущественно в орто- и пара-положения; соединения с электроноакцепторными заместителями в мета-положение. В большинстве случаев при сульфировании замещённых бензолов образуются смеси изомеров, соотношение которых зависит от природы заместителя, сульфирующего реагента и условий реакций (концентрации реагентов, температуры, растворители, наличия катализаторов и др.).
Сульфирование ароматических соединений
Путём подбора оптимальных условий возможно селективное сульфирование. Так, сульфирование толуола серной кислотой при 20 °С приводит к равным количествам орто- и пара-толуолсульфокислот, а при использовании SO3 в тех же условиях – исключительно к пара-изомеру; при сульфировании фенола при низких температурах преимущественно образуется о-фенолсульфокислота, тогда как при 100 °С – п-фенолсульфокислота. Как правило, подобные различия обусловлены превращением одних изомеров в другие, термодинамически более стабильные, благодаря изомеризации или обратимости сульфирования. Например, нафталин при температурах ниже 100 °С первоначально образует α-нафталинсульфокислоту, которая во времени превращается в β-изомер в результате последовательного десульфирования-ресульфирования. Сульфирование при 160 °С приводит исключительно к β-нафталинсульфокислоте.
Сульфирование гетероциклических соединений
Для сульфирования гетероциклических соединений (фуран, пиррол, тиофен, индол и др.) используют комплексы SO3 с диоксаном или пиридином. Эти же реагенты применяют для сульфирования алифатических соединений, содержащих сильные электроноакцепторные группы; при этом образуются, как правило, α-сульфопроизводные:
Повышение СН-кислотности алифатических соединений способствует тому, что последующее сульфирование протекает более однозначно, чем моносульфирование. Например, ацетальдегид и уксусная кислота с высоким выходом образуют соответствующие да- и трисульфосоединения:
Легко реагируют с SO3 и его комплексами алкены, которые образуют в зависимости от структуры и условий β- или δ- сультоны либо α, β- или β, γ-ненасыщенные сульфокислоты, а также β-гидроксисульфокислоты.
Прямое сульфирование алканов протекает с трудом и сопровождается, как правило, окислением. Подобные реакции редко используют для препаративных целей, но находят им практическое применение для сульфирования полимеров, например полиэтилена, с целью их модификации. Значительно легче сульфируются углеводороды при совместном действии SO2 и О2 (сульфо-окисление), а также SO2 и Сl2 (сульфохлорирование). Обе реакции имеют радикальный характер и инициируются пероксидами, ультрафиолетовым или γ- облучением.
Сульфирование органических соединений
Для сульфирования органических соединений широко используют H2SO3 и её производные. Гидросульфиты присоединяются к альдегидам и кетонам, а также в условиях радикального инициирования к алкенам и алкинам; взаимодействуют с трифенил- и три(п-толил)карбинолами; реагируют с оксиранами, тииранами с раскрытием кольца.
Диазоалканы сульфируют SO2 в присутствии воды, спиртов, тиолов и аминов, последовательное действие SO2 и галогена на реактивы Гриньяра приводит к сульфонил-галогенидам.
К косвенным методам сульфирования относят сульфометилирование, сульфоэтилирование.
Применение
Сульфирование используют при получении поверхностно-активных веществ, ионообменных мембран и смол, биологически активных веществ, красителей и др.
