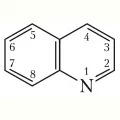
Хинолин
Хиноли́н (2,3-бензпиридин, бензопиридин, 1-беназин), гетероароматическое соединение, бензоконденсированный пиридин, C9H7N. Хинолин содержится в каменноугольной смоле. 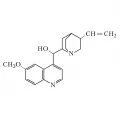 Структурная формула хинина.Структурное ядро хинолина присутствует в алкалоидах хинолинового ряда (хинин, цинхонидин, куспарин, эхинопсин, фагарин и др.). Впервые выделен из каменноугольной смолы немецким химиком-органиком Ф. Ф. Рунге в 1834 г. Молярная масса 129,17 /моль; плотность 1,095 г/см3; tплав –15,6 °C; tкип 237,7 °C.
Структурная формула хинина.Структурное ядро хинолина присутствует в алкалоидах хинолинового ряда (хинин, цинхонидин, куспарин, эхинопсин, фагарин и др.). Впервые выделен из каменноугольной смолы немецким химиком-органиком Ф. Ф. Рунге в 1834 г. Молярная масса 129,17 /моль; плотность 1,095 г/см3; tплав –15,6 °C; tкип 237,7 °C.
Физико-химические свойства
Хинолин – бесцветная маслянистая гигроскопичная жидкость с неприятным запахом, темнеющая на воздухе. Хинолин в любых соотношениях смешивается с этанолом, диэтиловым эфиром, сероуглеродом, ацетоном, бензолом; растворяется в воде [6 г/100 мл (20 °C)]; перегоняется с водяным паром.
Показатель константы кислотности (pKa) составляет 4,94.
С сильными кислотами хинолин образует соли, с алкилгалогенидами, диалкилсульфатами, ароматическими сульфоэфирами – четвертичные хинолиновые соли.
При каталитическом гидрировании хинолина образуется 1,2,3,4- или 5,6,7,8-тетрагидрохинолин, и далее декагидрохинолин. Окисление хинолина, в зависимости от условий реакции и природы используемого окислителя, приводит к получению 2-хинолинола, 2-хинолинона, 2,3-пиридиндикарбоновой кислоты, 8-оксихинолина, N-оксида хинолина или никотиновой кислоты.
Хинолин обладает многими свойствами соединений рядов бензола и пиридина. Нуклеофильное замещение происходит в основном в пиридиновом кольце, электрофильное – в бензольном. Галогенирование хинолина идёт преимущественно в положение 3. При нитровании без нагревания в концентрированной серной кислоте образуется смесь 5- и 8-нитрохинолинов, горячей азотной кислотой – 5,7- или 6,8-динитрохинолин, диоксидом азота – 7-нитрохинолин. Сульфирование концентрированной серной кислотой при 230 °C идёт в положение 5, при 300 °C – в положение 6. Дымящая серная кислота сульфирует в положения 5 и 8. В реакции с аммиаком в присутствии никеля Ренея образуется 2-аминохинолин. Алкилирование и арилирование реактивами Гриньяра или литийорганическими соединениями проходит преимущественно в положение 2.
Способы получения
Хинолин выделяют из каменноугольной смолы или синтезируют по реакции Скраупа конденсацией анилина и глицерина в присутствии серной кислоты.
Применение
Хинолин и его производные используют как сырьё в органическом синтезе, в фармацевтической промышленности, для синтеза цианиновых красителей. Хинолин применяется как растворитель и экстрактант для серы, фосфора, полициклических ароматических соединений.
Объём мирового рынка хинолина составил 341,2 млн долл. США в 2022 г. и, по прогнозу, вырастет до 498,1 млн долл. к концу 2033 г. (в среднем рост на 3,5 % в год) (Quinoline market // Future Market Insights).