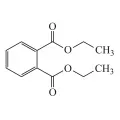
Диэтилфталат
Диэтилфтала́т (диэтиловый эфир фталевой кислоты, диэтил-1,2-бензолдикарбоксилат), органическое соединение, сложный эфир фталевой кислоты, С6Н4(СООС2Н5)2. Диэтилфталат может вызывать функциональные изменения центральной и периферической нервной системы. Молярная масса 222,24 г/моль; плотность 1,118 г/см3, 1,232 г/см3 (при 14 °C); tпл –40,5 °C; tкип 298–299 °C.
Физико-химические свойства
Диэтилфталат – бесцветная жидкость без запаха, обладающая горьким вкусом, малорастворимая в воде [0,1 г/100 мл (18 °C), 0,15 г/100 мл (20 °C)], минеральных маслах (2,8 г/100 мл), растворимая в бензоле, ацетоне, хлороформе, в любых соотношениях смешивается с этанолом, диэтиловым эфиром. Совместим с эфирами целлюлозы, многими виниловыми полимерами.
Диэтилфталат обладает химическими свойствами сложных эфиров. Он медленно гидролизуется под действием влаги с образованием фталевой кислоты и этанола; реакция ускоряется основаниями и кислотами. При кипячении диэтилфталата с мочевиной или тиомочевиной и этилатом натрия в спиртовом растворе образуется фталимид. Нагревание диэтилфталата с сульфатом калия приводит к образованию фталевого ангидрида. При гидрировании диэтилфталата при высоком давлении на никеле Ренея получается смесь цис- и транс-гексагидродиэтилфталатов. При нагревании с этиленгликолем образуются полимеры гликольфталата. При конденсации диэтилфталата с этилацетатом в присутствии металлического натрия и последующем омылении промежуточного продукта получается индандион.
Способы получения
В промышленности диэтилфталат получают нагреванием этанола с фталевым ангидридом в присутствии небольших количеств серной кислоты в качестве катализатора.
Применение
Диэтилфталат используют как пластификатор полимеров, фиксатор запаха в парфюмерии, растворитель, репеллент. Он применяется для обезвоживания этанола, а также как денатурирующая добавка в этанол.