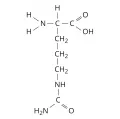
Цитруллин
Цитрулли́н (N-5-аминокарбонилорнитин, N-δ-карбамоилорнитин, 2-амино-5-уреидопентановая кислота, 2-амино-5-(карбамоиламино)пентановая кислота, α-амино-δ-уреидовалериановая кислота, общепринятое сокращение: Cit), непротеиногенная α-аминокислота, H2NC(O)NH(CH2)3CH(NH2)COOH. Содержит асимметрический атом углерода, обладает оптической активностью, может существовать в виде двух энантиомеров – D-цитруллина и L-цитруллина. В природе преобладает L-форма цитруллина. Молярная масса 175,19 г/моль. Плотность 0,8488 г/см3. Температура плавления 222 °C (с разложением).
Физико-химические свойства
Цитруллин – бесцветное кристаллическое вещество, растворимое в воде, нерастворимое в этаноле, метаноле, диэтиловом эфире.
Константы диссоциации кислоты (рКа) составляют 2,43 для карбоксильной группы (α-COOH) и 9,69 для аминогруппы (α-NH3+). При физиологических условиях цитруллин существует в виде цвиттер-иона.
Цитруллин устойчив к действию кислот, при обработке щёлочью разлагается на орнитин, мочевину и диоксид углерода. Он образует комплексы с металлами, вступает в реакции, характерные для карбоновых кислот и аминов, а именно: реакции этерификации, взаимодействие с аминами, декарбоксилирование, реакции с азотистой кислотой, окислительное деаминирование, переаминирование, N-алкилирование, N-ацилирование, образование пептидной связи.
Способы получения
L-цитруллин получают при обработке L-аргинина слабыми растворами щелочей.
Участие в обмене веществ
L-цитруллин – важный метаболит орнитинового цикла. L-орнитин-карбамоилтрансфераза (КФ 2.1.3.3) митохондрий печени переносит карбамоильную группу с карбамоилфосфата на L-орнитин с образованием L-цитруллина, который выходит в цитозоль. Далее в реакции, катализируемой аргининосукцинат-синтазой (КФ 6.3.4.5), к L-цитруллину присоединяется аминогруппа L-аспартата. Нарушения в работе ферментов цикла мочевины приводят к заболеваниям, сопровождающимся нарушением координации движений, раздражительностью, сонливостью, умственной отсталостью.
L-цитруллин образуется как побочный продукт при синтезе оксида азота (II) из L-аргинина под действием NO-синтазы (КФ 1.14.13.39).
В корневых клубеньках некоторых растений, например ольхи, реакция карбамоилирования L-орнитина с образованием L-цитруллина представляет собой основной путь фиксации азота.
В белках L-цитруллин появляется в результате посттрансляционной модификации L-аргинина под действием протеинаргинин деиминазы (КФ 3.5.3.15). Этой модификации подвергаются белки, участвующие в кератинизации, основной белок миелина. Нарушения в образовании цитруллина в белках ассоциированы с аутоиммунными заболеваниями (например, ревматоидным артритом, рассеянным склерозом, псориазом). Цитруллинизация гистонов участвует в эпигенетической регуляции транскрипции генов.
Применение
В медицине используется как общетонизирующее средство в виде малата цитруллина.