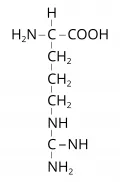
Аргинин
Аргини́н (α-амино-δ-гуанидил-н-валериановая кислота, 2-амино-5-гуанидинпентановая кислота, общепринятые сокращения: Arg, R, Арг), HN=C(NH2)NH(CH2)3CH(NH2)COOH, алифатическая α-аминокислота с выраженными основными свойствами (за счёт гуанидиновой группы). Содержит асимметрический атом углерода, обладает оптической активностью, существует в виде двух энантиомеров – L-аргинина и D-аргинина. В природе встречается преимущественно в форме L-изомера. Молярная масса 174,2 г/моль. Плотность 1,46 г/см3. Температура плавления 238 °C (с разложением). Впервые аргинин был выделен из проростков люпина (1886, Э. Шульце и Э. Штайгер). В 1899 г. Э. Шульце и Э. Винтерштайн синтезировали аргинин из орнитина и цианамида.
L-аргинин – протеиногенная аминокислота, кодируется триплетами CGU, CGC, CGA, CGG, AGA и AGG. Входит в состав белков (частота встречаемости 5,90) и пептидов, присутствует в большом количестве в резервных белках и зародышевых органах растений, участвует в синтезе многих биологически активных соединений, в том числе оксида азота (II), стимулирует образование цитокинов, высвобождение гормонов.
L-аргинин – условно незаменимая аминокислота, он в достаточных количествах синтезируется в организме здорового взрослого человека, однако дополнительное потребление его с пищей необходимо для детей, подростков, пожилых и больных людей, при травмах, ожогах.
Физико-химические свойства
Аргинин – бесцветное кристаллическое вещество. L-аргинин растворим в воде [15 г/100 мл (21 °C)], малорастворим в этаноле, нерастворим в диэтиловом эфире. DL-аргинин растворим в воде, нерастворим в этаноле, диэтиловом эфире, бензоле.
В слабощелочных и нейтральных растворах аргинин существует в виде цвиттер-иона. Его изоэлектрическая точка равна 10,76. Константы диссоциации кислоты (рКа) составляют 2,17 для карбоксильной группы (α-COOH), 9,04 для аминогруппы (α-NH3+) и 12,84 для гуанидиновой группы.
Аргинин взаимодействует с кислотами и щелочами, образует комплексы с металлами, вступает в реакции, характерные для карбоновых кислот и аминов: реакции этерификации, взаимодействие с аминами, декарбоксилирование, реакции с азотистой кислотой, окислительное дезаминирование, переаминирование, N-алкилирование, N-ацилирование, образование пептидной связи. Гуанидиновая группа аргинина легко отщепляется при гидролизе в избытке гидроксида бария при 100 °С с образованием мочевины и орнитина. При обработке аргинина эквимолекулярным количеством водного раствора Ва(ОН)2 отщепляется аммиак с образованием цитруллина.
Качественной реакцией на аргинин является реакция Сакагучи: в щелочной среде при взаимодействии с α-нафтолом и гипохлоритом или гипобромитом натрия аргинин даёт ярко-красное окрашивание.
Способы получения
Производство L-аргинина осуществляется экстракцией из белковых гидролизатов и при помощи микробного синтеза.
Участие в обмене веществ
Биосинтез L-аргинина происходит в реакциях орнитинового цикла. Эндогенный синтез L-аргинина осуществляется главным образом под действием аргининосукцинатсинтазы (КФ 6.3.4.5) и аргининосукцинатлиазы (КФ 4.3.2.1) из цитруллина. Синтез L-аргинина также возможен из орнитина и L-пролина.
L-аргинин входит в состав молекул белков (до 85 % в протаминах, до 15,9 % в гистонах, до 8,3 % в желатине) и пептидов (например, тафцина – тетрапептида с выраженным иммуномодуляторным действием). Значительное количество L-аргинина присутствует в растениях [в том числе красных водорослях, тыквенных (до 15 % в семенах)], особенно в резервных белках и зародышевых органах.
L-аргинин участвует в синтезе мочевины и орнитина в орнитиновом цикле, значительные количества L-аргинина в клетке расходуются на синтез креатина – важного участника энергетического обмена. L-аргинин участвует также в синтезе полиаминов, которые содействуют пролиферации и дифференцировке, ингибируют апоптоз клеток.
Существенная доля L-аргинина в организме идёт на синтез оксида азота (II), который усиливается в условиях индукции соответствующей синтазы оксида азота (NO-синтазы) при воспалительных процессах, сепсисе и других патологиях. Оксид азота (II) обеспечивает синаптическую пластичность в центральной нервной системе, участвует в регуляции кровяного давления, релаксации гладкой мускулатуры. За открытие роли оксида азота как сигнальной молекулы в регуляции сердечно-сосудистой системы Р. Феркготт, Л. Игнарро и Ф. Мьюрад в 1998 г. были удостоены Нобелевской премии по физиологии или медицине.
L-аргинин стимулирует образование ряда цитокинов, а также высвобождение из гипофиза гормона роста и пролактина, а из поджелудочной железы – глюкагона и инсулина; активирует углеводный и липидный обмен.
Применение
L-аргинин применяется в медицине в составе средств парентерального питания и ноотропных средств.