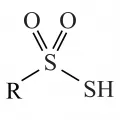
Тиосульфокисло́ты (тиолсульфоновые кислоты), соединения общей формулы RSO2SH, где R – opганический остаток. Тиосульфокислоты – неустойчивые соединения, в свободном виде неизвестны. Выделены и изучены соли тиосульфокислот RSO2S–M+ (M – натрий, калий, серебро и другие металлы, аммоний), аминоэфиры RSO2SNR'R:, эфиры RSO2SR' (тиолсульфонаты, тиосульфонаты). Известны также тиолангидриды RSO2SSO2R, S-оксиды тиолсульфонатов RSO2S(O)R' и 1,2-дисульфоны RSO2SO2R'.
Соли тиосульфокислот – кристаллические вещества, умеренно растворимые в воде, этаноле; тиолсульфонаты – вязкие высококипящие жидкости (низшие эфиры) либо кристаллические вещества.
При действии кислот на соли тиосульфокислот не удаётся выделить свободные тиосульфокислоты, а лишь продукты их разложения: сульфиновые кислоты, серу, сероводород и др.
Из производных тиосульфокислот наиболее изучены тиолсульфонаты. Для них характерны реакции с нуклеофильными реагентами по сульфенильному атому серы, что позволяет использовать их как сульфенилирующие агенты:RSO2SR′+X−→RSO2_+R′SX,X=R′′O,R′′S,R2′′N и др.
Исключение составляют эфиры полифтортиолсульфокислот, которые при взаимодействии с аминами и тиолами образуют сульфоновые производные:
CF3SO2SR⟶R2′NHCF3SO2NR2′+RSH;
CF3SO2SR⟶R′SHCF3SO2SR′+RSH.
При гидролизе тиолсульфонатов в присутствии оснований образуются соли сульфиновых кислот и дисульфиды:
3RSO2SR′⟶4OH−3RSO2_+R′SO2_+R′SSR′+2H2O.
Восстановление тиолсульфонатов приводит, в зависимости от используемых реагентов, к сульфонам, сульфиновым кислотам, дисульфидам и тиолам:
RSO2SR′⟶[(C2H5)2N]3PRSO2R′+[(C2H5)N]3PS;
RSO2SR′⟶Zn−C2H5OHRSO2H+R′SH;
RSO2SR′⟶2Ph3PRSSR′+2Ph3PO;
RSO2SR′⟶Zn−HClRSH+R′SH.
При осторожном окислении тиолсульфонатов перекисью водорода получаются 1,2-дисульфоны, в более жёстких условиях происходит разрыв связи S−S и образуются сульфоновые кислоты:
RSO2SR′⟶H2O2RSO2SO2R′+2H2O;
RSO2SR′⟶H2O2RSO2OH+R′SO2OH.
Тиосульфокислоты в виде их солей получают взаимодействием хлорангидридов сульфокислот с тиолатами щелочных или щёлочноземельных металлов, либо солей сульфиновых кислот с элементарной серой, например:
RSO2Cl+2MSH−MCl⟶RSO2SM,M=K,Na,Ca,Ba;
ArSO2Na+S8⟶NH3ArSO2SNa.
Тиолсульфонаты получают контролируемым окислением дисульфидов надкислотами, азотной кислотой, перекисью водорода, оксидом ванадия(V), хлором в уксусной кислоте; взаимодействием солей сульфиновых кислот с сульфенилгалогенидами; расщеплением сульфидов арилсульфиновыми кислотами:
RSSR′⟶[O]RSO2SR′;
RSO2M+R′SHal−MHal⟶RSO2SR′,M=K,Na,Ag;
RCH2SCH2R+3ArSO2H−H2O⟶H+ArSO2SCH2R+ArSO2SAr+RCHO.
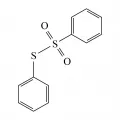 Фунгицид S-фенилбензолтиосульфонат.Фунгицид S-фенилбензолтиосульфонат.Многие производные тиосульфокислот обладают бактерицидным и фунгицидным действием. Соли и эфиры тиосульфокислот применяют в качестве вулканизаторов каучуков, промежуточных продуктов в синтезе лекарств и фунгицидов.
Фунгицид S-фенилбензолтиосульфонат.Фунгицид S-фенилбензолтиосульфонат.Многие производные тиосульфокислот обладают бактерицидным и фунгицидным действием. Соли и эфиры тиосульфокислот применяют в качестве вулканизаторов каучуков, промежуточных продуктов в синтезе лекарств и фунгицидов.
И. И. Крылов. Первая публикация: Химическая энциклопедия, 1995. Фунгицид S-фенилбензолтиосульфонат.Многие производные тиосульфокислот обладают бактерицидным и фунгицидным действием. Соли и эфиры тиосульфокислот применяют в качестве вулканизаторов каучуков, промежуточных продуктов в синтезе лекарств и фунгицидов.
Фунгицид S-фенилбензолтиосульфонат.Многие производные тиосульфокислот обладают бактерицидным и фунгицидным действием. Соли и эфиры тиосульфокислот применяют в качестве вулканизаторов каучуков, промежуточных продуктов в синтезе лекарств и фунгицидов.