Сульфоны
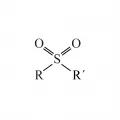
Сульфо́ны, сераорганические соединения общей формулы RR′SO2 (R, R′ – алкил, арил и др.). В природе встречаются редко, диметилсульфон (CH3)2SO2 найден в хвоще, в крови и надпочечниках некоторых животных. Преимущественно малотоксичны, за исключением дивинилсульфона (CH2=CH)2SO2, обладающего кожно-нарывным действием.
Физико-химические свойства
Сульфоны – бесцветные, не имеющие запаха кристаллические вещества или малолетучие жидкости, растворимые во многих органических растворителях; некоторые низкомолекулярные сульфоны растворяются в воде.
Свойства некоторых сульфонов
Соединение | Молярная масса (г/моль) | tпл (°C) | tкип (°C) | Растворимость |
Диметилсульфон (метилсульфон, метилсульфанилметан), (CH3)2SO2 | 94,13 | 109 | 235, 238 | Растворим в воде, этаноле, бензоле |
Диэтилсульфон (этилсульфон, этилсульфонилэтан) (C2H5)2SO2 | 122,18 | 70, 73–74 | 248 | Растворим в воде (15,6 г/100 мл), горячем диэтиловом эфире, хорошо растворим в бензоле, петролейном эфире |
Дипропилсульфон (пропилсульфон, 1-пропилсульфонилпропан) (CH3CH2CH2)2SO2 | 150,24 | 29–30 | – | Растворим в этаноле, диэтиловом эфире, плохо растворим в воде |
Дибутилсульфон (бутилсульфон, 1-бутилсульфонилбутан) (C4H9)2SO2 | 178,29 | 43 | – | Растворим в этаноле, диэтиловом эфире, нерастворим в воде |
Дифенилсульфон (фенилсульфон, фенилсульфонилбензол, бензолсульфон, сульфобензид) (C6H5)2SO2 | 218,27 | 128–129 | 377,8 | Растворим в этаноле, диэтиловом эфире, бензоле, плохо растворим в воде |
Дибензилсульфон (бензилсульфон) (C6H5CH2)2SO2 | 246,33 | 151 | 290 (с разложением) | Хорошо растворим в ацетоне, растворим в горячей воде, бензоле, уксусной кислоте, плохо растворим в этаноле |
Бензидилсульфон (дибензтиофен-2,7-диамино-9-диоксид, 2,7,-диаминодифениленсульфон) (NH2C6H3)2SO2 | 246,28 | 327–328 | – | Нерастворим в воде, этаноле, диэтиловом эфире |
Сульфонал (ацетодиэтилсульфон, диэтилсульфондиметилметан) (CH3)2C(SO2C2H5)2 | 228,32 | 126 | 360 | Плохо растворим в воде, растворим в этаноле, диэтиловом эфире |
Трионал [метилсульфонал, 2,2-бис-(этилсульфонил)-бутан] C2H5(CH3)C(SO2C2H5)2 | 242,35 | 74–76 | разлагается | Плохо растворим в воде (0,3 г/100 мл), растворим в этаноле (5,7 г/100 мл), диэтиловом эфире [4,71 г/100 мл (15 °C)] |
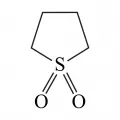
Сульфолан (тетраметиленсульфон, тиолан-1,1-диоксид, 2,3,4,5-тетрагидротиофен-1,1-диоксид) C4H8SO2 | 120,17 | 28,4 | 285 (с разложением) | Растворим в воде, спиртах, хлороформе, четырёххлористом углероде |
Дивинилсульфон (винилсульфон) (CH2=CH2)2SO2 | 118,16 | –16 |
| Плохо растворим в воде, хорошо растворим в органических растворителях |
Сульфоны – химически и термически стабильные соединения.
Циклические сульфоны под действием сильных восстановителей (например, тетрагидридоалюмината лития в диэтиловом эфире) превращаются в сульфиды. Сульфоны элиминируют молекулу оксида серы(IV) при облучении ультрафиолетовым светом, нагревании или под действием некоторых восстановителей. В щелочных условиях сульфоны подвергаются 1,2-элиминированию с образованием сульфинат-ионов. По α-положению сульфоны взаимодействуют с диазометаном, карбонильными, галогенсодержащими и другими соединениями. Ароматические сульфоны под действием литийорганических соединений подвергаются внутримолекулярной перегруппировке с образованием бензилсульфиновых кислот (перегруппировка Смайлса).
Способы получения
Сульфоны получают окислением сульфидов или сульфоксидов (окислители – пероксид водорода в уксусной кислоте, перманганат калия, бихромат натрия и др.); алкилированием или арилированием сульфиновых кислот или сульфинатов; термической перегруппировкой аллилсульфинатов; свободнорадикальным присоединением сульфонилгалогенидов к ненасыщенным соединениям; циклоприсоединением оксида серы(IV) к диенам; взаимодействием сульфенов с алкенами. Диарил- и алкиларилсульфоны получают взаимодействием сульфонилгалогенидов с ароматическими соединениями (реакция Фриделя – Крафтса).
Применение
Сульфоны применяют в производстве лекарств, пестицидов, красителей и др.; на основе ариленсульфонов изготавливают конструкционные и электротехнические пластмассы. Некоторые сульфоны (например, сульфолан) используют как растворители; противомикробные средства (дапсон); седативные средства (сульфонал, трионал, тетронал).