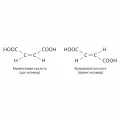
Малеиновая и фумаровая кислоты
Малеи́новая и фума́ровая кисло́ты, цис- и транс-изомеры этилен-1,2-дикарбоновой кислоты (бутен-1,4-диовой кислоты), простейшего представителя непредельных дикарбоновых кислот, НООССН═СНСООН. Молярная масса 116,07 г/моль. Плотность 1,59 г/см3 и 1,635 г/см3 для малеиновой и фумаровой кислот соответственно. Температура плавления 130 °C (с разложением) для малеиновой кислоты, 287 °C (в запаянном капилляре) для фумаровой кислоты. Малеиновая кислота впервые была получена Ж. Л. Лассенем в 1819 г. перегонкой яблочной кислоты.
Физико-химические свойства
Малеиновая и фумаровая кислоты – бесцветные кристаллические вещества. Малеиновая кислота растворима в воде [78,8 г/100 мл (25 °C), 392,6 г/100 мл (97,5 °C)], этаноле [69,9 г/100 мл (20 °C)], диэтиловом эфире [8 г/100 мл (25 °C)], ледяной уксусной кислоте, ацетоне, малорастворима в бензоле. Фумаровая кислота растворима в воде [0,7 г/100 мл (25 °C), 9,8 г/100 мл (100 °C)], этаноле [5,75 г/100 мл (29,7 °C), 4,76 г/100 мл (76 °C)], диэтиловом эфире [0,72 г/100 мл (25 °C)], концентрированной серной кислоте, малорастворима в хлороформе, четырёххлористом углероде и ацетоне, нерастворима в бензоле.
Фумаровая кислота обладает более слабыми кислотными свойствами (константы диссоциации кислоты (pKa) для фумаровой кислоты составляют 3,02 и 4,38, для малеиновой – 1,9 и 6,07) и большей устойчивостью, чем малеиновая кислота. На свету, при нагревании выше 200 °С или при действии химических реагентов малеиновая кислота изомеризуется в фумаровую. На примере малеиновой и фумаровой кислот Й. Вислиценус в 1887 г. впервые обнаружил существование геометрической изомерии соединений с двойной связью.
Фумаровая и малеиновая кислоты обладают свойствами α,β-ненасыщенных карбоновых кислот. Оба изомера легко восстанавливаются до янтарной кислоты, окисляются пероксидами в DL-винную или в мезовинную кислоту, озоном – в глиоксиловую и щавелевую кислоты, вступают в диеновый синтез, при их взаимодействии с водой, хлорноватистой кислотой или галогенами образуются яблочная, хлоряблочная и дигалогенянтарная кислоты соответственно, с одноатомными спиртами – моно- и диэфиры, с аммиаком и аминами – диамиды аминоянтарной кислоты, с ненасыщенными соединениями под действием УФ-облучения в присутствии фотосенсибилизаторов – производные циклобутана. Малеиновая кислота под действием дегидратирующих реагентов (оксид фосфора (V), ацетилхлорид и др.) или при нагревании выше 130 °С превращается в малеиновый ангидрид, при нагревании в присутствии хинолина или оксида меди (I) образуется акриловая кислота. Соли и эфиры малеиновой кислоты называются малеинатами, фумаровой кислоты – фумаратами.
Способы получения
Фумаровая кислота получается при окислении фурфурола хлоратом натрия в присутствии ванадиевого катализатора, дегидратации яблочной кислоты или дегидробромировании бромянтарной кислоты.
В промышленности малеиновую кислоту получают гидролизом малеинового ангидрида, фумаровую кислоту – изомеризацией малеиновой кислоты под действием соляной кислоты и соединений брома.
Участие в обмене веществ
Малеиновая кислота в природе не найдена. Фумаровая кислота обнаружена в растениях, грибах, лишайниках.
В цикле трикарбоновых кислот фумарат образуется при дегидрировании сукцината сукцинатдегидрогеназой (КФ 1.3.5.1). Следующим шагом фумаратгидратаза (КФ 4.2.1.2) осуществляет гидратацию фумарата до L-малата.
С орнитиновым циклом сопряжён цикл регенерации аспартата из фумарата. Образовавшийся из аргининосукцината под действием аргининосукцинат-лиазы (КФ 4.3.2.1) фумарат включается в реакции цитратного цикла и превращается в оксалоацетат, который путём трансаминирования вновь образует аспартат.
Фумарат образуется в процессе встречающегося в основном у бактерий и грибов неокислительного деаминирования аспарагиновой кислоты под действием фермента L-аспартатаммиаклиаза (КФ 4.3.1.1).
Фумарат является одним из продуктов катаболизма L-фенилаланина и L-тирозина.
Применение
Малеиновая кислота применяется в производстве винной и яблочной кислот, ПАВ, полимерных материалов, алкидных смол, фумаровая кислота – в производстве полиэфирных смол, синтетических высыхающих масел, пластификаторов, а также как заменитель лимонной и винной кислот в пищевой промышленности (пищевая добавка E297), фумараты – в медицине.