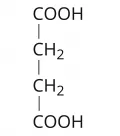
Янтарная кислота
Янта́рная кислота́ (1,4-бутандикарбоновая кислота, бутандиовая кислота), двухосновная насыщенная алифатическая карбоновая кислота, HOOC(CH2)2COOH. В живых организмах встречается в виде аниона – сукцината (от лат. succinum – янтарь). Сукцинат является промежуточным продуктом цикла трикарбоновых кислот, катаболизма γ-аминобутирата, участвует в биосинтезе гема. В небольших количествах янтарная кислота содержится во многих растениях, смолах (в том числе янтаре), буром угле. Молярная масса 118,09 г/моль. Плотность 1,564 г/см3. Температура плавления 185 °C. Температура кипения 235 °C.
Физико-химические свойства
Янтарная кислота – бесцветное кристаллическое вещество, растворимое в воде [6,8 г/100 мл (20 °C), 121 г/100 мл (100 °C)], этаноле [9,9 г/100 мл (5 °C), 7,5 г/100 мл (21,5 °C)], диэтиловом эфире [1,2 г/100 мл (15 °C)], метаноле, ацетоне, нерастворимое в бензоле, толуоле, хлороформе. Константа диссоциации кислоты (рКа) составляет 4,21 и 5,72.
Обладает химическими свойствами карбоновых кислот, образует два ряда производных: кислые или средние соли, полные и неполные эфиры, амиды, галогенангидриды и др. При температуре выше 235 °C, отщепляя воду, образует янтарный ангидрид, при нагревании с аммиаком и аминами даёт сукцинимид и его N-производные.
Способы получения
Янтарную кислоту получают как побочный продукт при производстве адипиновой кислоты, при гидрировании малеинового ангидрида, при окислении углеводородов С4–С10 выделяют из смеси образующихся кислот. Возможен также микробиологический синтез янтарной кислоты.
Участие в обмене веществ
Янтарная кислота (сукцинат) в ходе цикла трикарбоновых кислот образуется при гидролизе сукцинильного производного кофермента А (сукцинил-КоА) под действием фермента сукцинат-КоА-лигазы (КФ 6.2.1.4). Далее сукцинатдегидрогеназа (КФ 1.3.5.1) окисляет сукцинат в фумарат. Сукцинат является продуктом катаболизма γ-аминобутирата. Производное янтарной кислоты сукцинил-КоА участвует в синтезе порфиринов – предшественников гема и хлорофилла.
В клетках растений, некоторых беспозвоночных и ряда бактерий сукцинат образуется в ходе глиоксилатного цикла в результате расщепления изоцитрата изоцитратлиазой (КФ 4.1.3.1).
Применение
В химической промышленности янтарную кислоту применяют в производстве инсектицидов, красителей, лекарств, алкидных смол и др. Эфиры используют в пищевой и парфюмерной промышленности.
Янтарная кислота является пищевой добавкой E363 (регулятор кислотности).
В медицинских целях янтарную кислоту используют как средство, снижающее гипоксию и улучшающее энергообеспечение и метаболизм тканей.