Трифторметансульфокислота
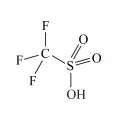
Трифторметансульфокислота́ (трифторметансульфоновая кислота, трифлик кислота, ТФМСК), фторорганическое соединение, перфторалкансульфокислота, CF3SO2OH. Соли и эфиры трифторметансульфокислоты называются трифлатами или трифторметилсульфонатами. Впервые синтез трифторметансульфокислоты описан в 1954 г. Р. Н. Хазелдином и Дж. М. Киддом; она была получена окислением трифторметилмеркаптида ртути водным раствором пероксида водорода. Молярная масса 150,07 г/моль; плотность 1,696 г/см3; tпл –40 °C; tкип 162 °C.
Физико-химические свойства
Трифторметансульфокислота – прозрачная бесцветная жидкость с резким запахом, хорошо растворимая в полярных органических растворителях (диметилформамиде, диметилсульфоксиде, ацетонитриле и др.). В любых отношениях смешивается с водой. Гигроскопична. Дымит во влажном воздухе. Образует моногидрат.
Одна из самых сильных кислот (суперкислота) с функцией кислотности Гаммета H0 равной –14,1.
Трифторметансульфокислота и её сопряжённое основание обладают высокой термостабильностью и устойчивостью к восстановлению и окислению.
Трифторметансульфокислота образует соли, эфиры, ангидриды и галогенангидриды. Смешанные ангидриды трифторметансульфокислоты и карбоновых кислот служат хорошими ацилирующими агентами в реакции Фриделя – Крафтса.
Способы получения
В промышленности трифторметансульфокислоту получают электрохимическим фторированием метансульфохлорида (метансульфофторида) или метансульфокислоты в безводном фтористом водороде.
Применение
Трифторметансульфокислота используется в реакциях алкилирования и ацилирования Фриделя – Крафтса, как катализатор в реакциях циклизации, полимеризации и изомеризации углеводородов, как промежуточное соединение для органического синтеза в химической промышленности, фармацевтике, агрохимии.