Нафтолы
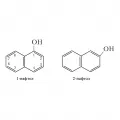
Нафто́лы (гидроксинафталины), производные нафталина общей формулы C10H8–n(OH)n, где n – 1, 2, 3 и более. Практическое значение имеют в основном нафтолы, содержащие гидроксильные группы в положении 1 (1-нафтол или α-нафтол) или 2 (2-нафтол или β-нафтол).
Физико-химические свойства
Нафтолы – бесцветные кристаллы с характерным запахом, хорошо растворимые в этаноле, диэтиловом эфире, ацетоне, бензоле, хлороформе, растворах щелочей, плохо – в воде; tпл 1-нафтола 96 °C, 2-нафтола 122 °C. В небольших количествах присутствуют в каменноугольной смоле.
Нафтолы легко вступают в реакции электрофильного замещения (галогенирования, сульфирования, нитрования). В водных растворах щелочей образуют соли, с ангидридами и хлорангидридами органических кислот – ацильные производные, со спиртами в присутствии соляной кислоты HCl или серной кислоты H2SO4 – простые эфиры; при нагревании с гидросульфитом натрия NaHSO3 – гидросульфитные производные, которые в присутствии избытка аммиака NH3 превращаются в нафтиламины. Каталитическое гидрирование в кислой среде (платина Pt, 70 °C) приводит к превращению 1- и 2-нафтолов в 5- и 6-гидрокситетралины, в щелочной среде (никель Ni или палладий Pd, 60 °C) – к 1- и 2-гидрокситетралинам; натриевые соли нафтолов при нагревании (130–170 °C) в атмосфере углекислого газа CO2 образуют 1(2)-гидроксинафталин-2(1)-карбоновые кислоты.
Получение
1-Нафтол получают гидролизом 1-нафтиламина или 5-аминонафталин-1-сульфокислоты, а также окислением тетралина с последующим дегидрированием; 2-нафтол – щелочным плавлением нафталин-2-сульфокислоты, окислением 1-изопропил-2-нафтиламина, а также гидролизом 2-хлорнафталина.
Применение
Применяют нафтолы в производстве нафтолсульфокислот, азокрасителей, в качестве антиоксидантов, антисептиков, как полупродукты органического синтеза. 2-Нафтол слабо раздражает кожу и слизистые оболочки дыхательных путей и глаз.