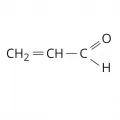
Акролеин
Акролеи́н (акриловый альдегид, акрилальдегид, пропеналь, проп-2-ен-1-аль), простейший ненасыщенный альдегид, CH2=CH-CHO. Выделен в 1843 г. Й. Редтенбахером при сухой перегонке жиров. Молярная масса 56,05 г/моль. Плотность 0,841 г/см3. Температура плавления от –88 до –86,5 °C. Температура кипения 52,5–53,5 °C.
Физико-химические свойства
Акролеин – бесцветная, легко воспламеняющаяся слезоточивая жидкость с резким запахом, хорошо растворимая в воде [40 г/100 мл (20 °C)] и во многих органических растворителях (этаноле, диэтиловом эфире, ацетоне).
Акролеин вступает в реакции, характерные для альдегидов и алкенов. Как альдегид, при взаимодействии со спиртами акролеин даёт ацетали. При взаимодействии акролеина с синильной кислотой образуется 2-гидрокси-3-бутеннитрил, с гидроксиламином – оксим, с реактивом Гриньяра – спирт. По месту двойной связи акролеин присоединяет галогеноводороды, галогены, воду, аммиак и амины, спирты и фенолы, тиолы, участвует в диеновом синтезе и как диен, и как диенофил. Кроме того, на химические свойства акролеина влияет наличие сопряжённых C=C- и C=O-связей. Так, например, присоединение брома по двойной связи будет проходить менее активно, чем у алкенов. Бисульфит натрия присоединяется не только по карбонильной группе (C=O), но и по двойной связи.
Окисление акролеина до акриловой кислоты возможно мягкими окислителями, например аммиакатом серебра. Окисление перекисью водорода приводит к образованию DL-глицеральдегида. При действии борогидрида натрия или алюминийгидрида лития на акролеин преимущественно восстанавливается карбонильная группа. При каталитическом гидрировании водородом C=C- и C=O-связи гидрируются независимо друг от друга с образованием аллилового спирта, пропионового альдегида и пропилового спирта.
При нагревании, под действием света или активаторов акролеин легко полимеризуется, для его стабилизации добавляют гидрохинон.
Акролеин раздражает слизистые оболочки глаз и дыхательных путей; токсичен. В быту образуется при термическом разложении жиров.
Способы получения
В промышленных условиях акролеин получают каталитическим окислением пропена воздухом. В лабораторных условиях акролеин также можно синтезировать из формальдегида и ацетальдегида, тетрагидрофурфурилового спирта, дегидратацией глицерина и др.
Применение
Акролеин применяют для получения DL-метионина, никотиновой и акриловой кислот, глицерина, DL-глицеральдегида, глутарового альдегида, 3-метилпиридина, фунгицидов, гербицидов, вкусовых и ароматических добавок, фармацевтических препаратов, в качестве мономера в производстве полимеров и сополимеров.