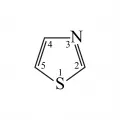
Тиазол
Тиазо́л (1,3-тиазол), гетероциклическое соединение, содержащее азот и серу, C3H3NS, молярная масса 85,13 г/моль.
Физико-химические свойства
Представляет собой бесцветную жидкость с запахом пиридина; растворяется в органических растворителях и в воде; tкип 115–118 °С; плотность 1,198 г/см3 (при 20 °С); показатель преломления 1,5969. Основание (рКа 2,53); для 4-метилтиазола рКа 3,07. Тиазол, как и другие азолы, – 6π-электронная гетероароматическая система. По химическим свойствам близок к пиридину и тиофену.
Производные тиазола обычно с трудом вступают в реакции электрофильного замещения, что обусловлено N-протонированием или комплексообразованием с кислотами Льюиса в условиях реакции. В условиях, исключающих эти реакции, бромирование Вr2 в бензоле и нитрование в уксусном ангидриде или тетрафтороборатом N-нитропиколиния в ацетонитриле идут в положение 5. Реакционная способность различных положений тиазольного цикла при электрофильном замещении, протекающем через катионный s-комплекс, уменьшается в ряду: 5→4–2-положение. Важную роль в химии тиазола играют реакции электрофильного замещения, идущие по т. н. илидному механизму, например реакция изотопного обмена:
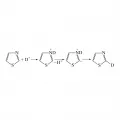 Реакция изотопного обмена.В реакциях нуклеофильного замещения наиболее активно положение 2, по которому протекают прямое нуклеофильное замещение атома водорода на аминогруппу по реакции Чичибабина и металлирование.
Реакция изотопного обмена.В реакциях нуклеофильного замещения наиболее активно положение 2, по которому протекают прямое нуклеофильное замещение атома водорода на аминогруппу по реакции Чичибабина и металлирование.
Под действием окислителей (например, надкислот) тиазол и его замещённые окисляются в соответствующие N-оксиды, способные к 1,3-диполярному присоединению. Тиазол и его производные устойчивы к действию водорода в момент выделения, а также в присутствии катализаторов, однако под действием борогидрида натрия NaBH4 превращаются в тетрагидротиазолы (тиазолидины). При действии никеля Ренея претерпевают десульфуризацию с образованием алифатических соединений.
Важное синтетическое значение имеет подвижность атома водорода метильной группы в положении 2 тиазолиевых солей, которая используется в синтезе цианиновых красителей, например по реакции:
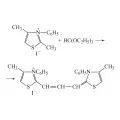 Синтез цианиновых красителей.
Синтез цианиновых красителей.
Получение
Основые методы синтеза тиазола и его замещённых: взаимодействием ɑ-галогенкетонов или ɑ-галогенальдегидов с тиоамидами (см. Синтезы Ганча), циклизация ɑ-тиоцианокетонов под действием водных растворов кислот или безводного хлороводорода НСl либо оксихлорида фосфора РОСl3, взаимодействием ациламинокарбонильных соединений с декасульфидом тетрафосфора P2S5, например:
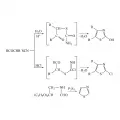 Реакции синтеза тиазола.
Реакции синтеза тиазола.
Применение
Важнейшее природное соединения ряда тиазолов – тиамин (витамин В1), молекула которого включает фрагмент соли тиазолия. Многие производные тиазола – лекарственные препараты, например норсульфазол – 2-сульфаниламидотиазол и фталазол [2-(N-о-карбоксибензоилсульфанил)амидотиазол]. Тиазолидиновое кольцо – структурный фрагмент пенициллина и разнообразных полусинтетических пенициллинов. Некоторые производные тиазола – красители, используемые в том числе и в цветной фотографии.