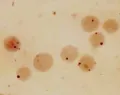
Анаплазмоз
Анаплазмо́з (Anaplasmosis), остро, подостро и хронически протекающая природно-очаговая трансмиссивная болезнь крупного и мелкого рогатого скота, вызываемая облигатными внутриэритроцитарными микроорганизмами Anaplasma. У крупного рогатого скота паразитируют виды Anaplasma marginale, Anaplasma сentrale, у коз и овец – Anaplasma ovis. Болезнь характеризуется лихорадкой непостоянного типа, анемией, истощением, снижением молочной и мясной продуктивности, гибелью молодняка, достигающей 50–80 %. Характерной особенностью анаплазмоза является длительное, практически пожизненное паразитоносительство переболевших животных, во время которого возможны рецидивы, обусловленные снижением резистентности организма из-за недостатка микроэлементов и витаминов, неполноценного питания, стрессовых состояний.
Болезнь была установлена в США у крупного рогатого скота в 1893 г., исследователи Т. Смит и Ф. Кильборн приняли анаплазм за одну из форм развития Piroplasma bigeminum. А. Тайлер в 1906 г. сначала рассматривал анаплазму как стадию развития Theileria mutans, а затем, в 1910 г. предложил назвать этого паразита Anaplasma marginale.
Источниками анаплазм являются больные животные и анаплазмоносители. К переносчикам анаплазм относят 22 вида клещей из семейства Ixodidae и 2 вида из семейства Argasidae (Argus persicus и Ornithodoros lahorensis), которые передают анаплазм трансовариально, трансфазно и путём прерывистого питания имаго – самцов (в пределах одной фазы клеща со слюной) Также переносчиками анаплазм могут быть кровососущие насекомые – слепни, комары, мухи-жигалки и овечья кровососка. Механическая передача возбудителя от заражённых животных к здоровым возможна через нестерильные инструменты при проведении зоотехнических мероприятий (взятие крови, вакцинация, обрезка рогов и т. д). Заражению анаплазмозом подвержены дикие жвачные, в том числе буйволы, бизоны, белохвостые олени, мулы, антилопы и др.
Анаплазмоз встречается повсеместно. Болезнь зарегистрирована на территории РФ [Башкортостан, Алтайский, Ставропольский, Краснодарский края, Калининградская, Ленинградская, Рязанская, Калужская, Московская, Тверская, Брянская, Смоленская, Владимирская области, республики Северного Кавказа (Дагестан, Ингушетия, Кабардино-Балкария, Карачаево-Черкесия, Северная Осетия – Алания, Чеченская Республика)]; в Белоруссии, Латвии, на Украине, в государствах Закавказья, Центральной Азии.
Размножение в позвоночном хозяине осуществляется простым бинарным делением или почкованием. При питании клеща на больном животном вместе с кровью анаплазмы проникают в кишечник клеща, где под воздействием ферментов кишечника они распадаются на субмикроскопические инициальные тела, которые в дальнейшем проникают в слюнные железы клеща.
Кровососущие насекомые (механические переносчики) могут переносить анаплазм от одних животных к другим в процессе питания кровью, однако в их организме они не размножаются, поэтому передача анаплазм должна произойти очень быстро – не позднее, чем через 5 мин после питания на больном животном. Существует и внутриутробная передача.
Патогенез
Возбудитель анаплазмоза в организме животного быстро размножается, поражая эритроциты. Основной и ведущий признак болезни – анемия, которая развивается на фоне лихорадки, угнетения, нарушения обмена веществ и функций сердечно-сосудистой системы (ССС) и желудочно-кишечного тракта (ЖКТ). В инкубационном периоде снижается число эритроцитов, возрастает количество лейкоцитов, наблюдается положительная реакция связывания комплемента (РСК). С развитием клинических признаков происходят сильные изменения в крови больных животных: появление молодых эритроцитов в крови, которые содержат меньше фосфолипидов, приводит к хрупкости эритроцитов, вследствие чего сокращается их жизнь до 15–22 дней, происходит усиление эритрофагоцитоза – количество эритроцитов снижается в 1,5–2 раза. В активизации эритрофагоцитоза важную роль играют аутоантитела. Размножение анаплазм в организме животного вызывают ответную реакцию клеток и тканей, которая сопровождается выработкой специфических антител, способствующих изъятию из крови поражённых анаплазмами эритроцитов и утилизации их в клетках (ретикулоэндотелиальная система). Большое количество поражённых эритроцитов фагоцитируется.
Возрастает потребление кислорода эритроцитами, поражёнными анаплазмами. Недостаток кислорода в эритроцитах приводит к гипоксии и гипоксемии, вследствие чего резко усиливается сердечная деятельность, учащается пульс и появляется аритмия, происходит нарушение процессов окисления и диссимиляции, результатом чего является прогрессирующее исхудание животного. Нарастание этих признаков при прогрессирующем исхудании приводит к смерти даже при снижении паразитемии.
Клиническая картина
Длительность инкубационного периода при анаплазмозе у животных различна и варьирует от 3 недель до 3 месяцев в зависимости от резистентности организма и многих факторов внешней среды.
Основными клиническими признаками являются резко выраженная анемия, лихорадка непостоянного типа, в тяжёлых случаях – высокая температура (до 42 °С), слабая иктеричность (желтушность) слизистых оболочек, прогрессирующее истощение, отёки, учащение дыхания, нарушения ССС и ЖКТ. Мочеиспускание частое, гемоглобинурия отсутствует. Животные истощены. Стельные коровы нередко абортируют. Наступают изменения в крови – анизоцитоз, пойкилоцитоз, базофильная зернистость эритроцитов, увеличение числа лимфоцитов и моноцитов, снижение количества гемоглобина, общий белок сыворотки крови уменьшается до 4,42–5,31 %.
Диагностика и лечение
Эффективность профилактики анаплазмоза прямо зависит от качества ранней диагностики болезни в хозяйстве и выявления животных-анаплазмоносителей, являющихся природным резервуаром инвазии. Рекомендовано в хозяйствах неблагополучных районов исследовать кровь всех животных серологически в реакции длительного связывания комплемента (РДСК), сочетая это исследование с определением уровня гемоглобина в крови. Все больные и переболевшие животные дают положительные реакции, титр колеблется в пределах от 1:80 до 1:280 и выше. У паразитоносителей титр 1:10, 1:50, реже более высокий.
У всех животных, положительно прореагировавших в РДСК, или с пониженным содержанием гемоглобина необходимо исследовать мазки крови на наличие анаплазм.
Мазки крови для исследования красятся по Романовскому – Гимзе. В каждом мазке необходимо просматривать не менее 100 полей зрения. Как правило, процент поражения эритроцитов варьируется от единичных до 30–40 %.
Анаплазмоз дифференцируют от тейлериоза, бабезиоза, лептоспироза. Нередко анаплазмоз проявляется вслед за этими болезнями и осложняет их.
При анаплазмозе животных лечение проводится комплексно и является как симптоматическим, так и специфическим.
Больных оставляют в помещениях и назначают диетические корма. В качестве симптоматических средств при запорах дают глауберову соль, эмульсии из растительных масел, а затем препараты, стимулирующие деятельность ЖКТ, – молочную кислоту, чемерицу, гидролизин. Для стимуляции кроветворения назначают микроэлементы в виде солей: сернокислую медь 1–2 мг/кг, хлористый кобальт 2–3 мл/100 кг веса в течение 10 дней внутрь в виде растворов, а также инъекции витаминов группы B (B1, B12). Слабым животным при нарушении сердечной деятельности следует вводить кофеин или камфару.
При анаплазмозе в качестве специфического лечения используются антибиотики тетрациклинового ряда [тетрациклин, хлортетрациклин (биомицин), окситетрациклин (террамицин)]. Эффективен «Нитокс 200» – пролонгированная форма на основе антибиотика окситетрациклина дигидрата. В препарате окситетрациклин находится в виде комплекса с магнием, что обусловливает его длительное пролонгированное действие. При внутримышечном применении препарат быстро всасывается и достигает максимальной концентрации в тканях примерно через 30–50 мин после введения. Препарат вводят однократно глубоко внутримышечно в дозе 1 мл на 10 кг живой массы. Максимальная доза для введения в одну точку тела для крупного рогатого скота – 20 мл, для мелкого рогатого скота – 5 мл. При необходимости препарат вводят повторно через 72 ч.
Профилактика и меры борьбы
Для успешной профилактики анаплазмоза необходимо сочетание общих ветеринарно-санитарных мероприятий и специфических противоанаплазмозных мер.
Общехозяйственные мероприятия: регулярная дезинфекция стойл; агрокультурное улучшение пастбищ; агромелиоративные мероприятия с созданием системы искусственного травосева и окультуривания пастбищ; огораживание пастбищ с применением электропастуха для недопущения проникновения диких животных – переносчиков клещей на территорию хозяйств; регулярный ежемесячный осмотр пасущихся животных для определения заклещёванности; карантинирование вновь поступающих в хозяйство животных и недопущение перемещения животных-носителей.
Метод биоценотической деструкции – обработка животных инсектоакарицидными препаратами в определённые сроки (мустангом, фьюри, бутоксом, циперилом и др.).
Метод иммунной атаки заключается в двукратной иммунизации животных инактивированной вакциной после окончания пастбищного сезона, чтобы к наступлению нового пастбищного сезона успел выработаться устойчивый иммунитет. Фундаментальное значение приобретает защита крупного рогатого скота от анаплазмозной инфекции путём вакцинации, позволяющей стимулировать как неспецифический, так и специфический иммунитет у животных и тем самым добиться полного уничтожения возбудителя анаплазмоза сразу после проникновения его в организм.