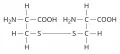
Цистин
Цисти́н (3,3´-дитио-бис-2-аминопропионовая кислота, β,β´-дитиодиаланин, дицистеин), HOOCCH(NH2)CH2SSCH2CH(NH2)COOH, алифатическая серосодержащая α-аминокислота, двухосновная диаминокислота. Содержит асимметрический атом углерода, обладает оптической активностью, может существовать в виде двух энантиомеров – D-цистина и L-цистина. В природе преобладает L-цистин. Кроме того, вследствие идентичности центров хиральности появляется оптически неактивный мезо-цистин. Впервые был выделен из мочевого песка (1810, У. Х. Волластон). Молярная масса 240,30 г/моль. Температура плавления 258–261°C (с разложением) для L-цистина, 247–249 °C для D-цистина, 225–227 °C для DL-цистина.
L-цистин – некодируемая аминокислота, образуется в результате ферментативного окисления L-цистеина. Участвует в формировании пространственной структуры белков и пептидов. L-цистин – заменимая для человека аминокислота, синтезируется в организме в достаточном количестве.
Физико-химические свойства
Цистин – бесцветное кристаллическое вещество, слабо растворимое воде [L-цистин, D-цистин 0,011 г/100 мл (25 °C), DL-цистин 0,006 г/100 мл (25 °C), L-цистин 0,052 г/100 мл (75 °C), L-цистин 0,11 г/100 мл (100 °C)], нерастворимое в этаноле, диэтиловом эфире, бензоле.
Как и другие аминокислоты, в кристаллах и полярных растворителях цистин существует в виде цвиттер-иона. Его изоэлектрическая точка равна 5,03. Константы диссоциации кислоты (рКа) составляют 1,04 и 2,05 для карбоксильных групп (α-COOH), 8,00 и 10,25 для аминогрупп (α-NH3+).
Дисульфидная связь цистина легко восстанавливается до сульфгидрильных групп под действием меркаптоэтанола или дитиотреитола. Так же легко проходит обратная реакция окисления под действием кислорода, особенно в слабощелочной среде.
Способы получения
Цистин обычно получают из продуктов гидролиза белков.
Участие в обмене веществ
L-цистин образуется в результате ферментативного окисления под действием цистинредуктазы (КФ 1.8.1.6) остатков двух молекул L-цистеина (в том числе из разных цепей) с образованием дисульфидных мостиков. Играет важную роль в формировании пространственных структур различных белков и биологически активных пептидов [например, инсулина (содержит 12,9 %), соматостатина, иммуноглобулинов], обусловливает характерные свойства (растворимость, растяжимость) таких фибриллярных белков, как кератин (содержание L-цистина в различных кератинах: волосы человека – 15,9 %, шерсть овцы – 11,1 %, шерсть собаки – 19,7 %), активность гормонов (окситоцин, вазопрессин, инсулин), ферментов (рибонуклеаза, химотрипсин и др.). Биосинтез и обмен L-цистина тесно связаны с L-цистеином, в организмах легко происходит их взаимное превращение.
С нарушениями метаболизма L-цистина связаны наследственные заболевания цистинурия и цистиноз.
Применение
L-цистин широко используется в медицинских целях. Лекарственные средства на основе L-цистина обладают антиоксидантным, детоксикационным, гепатотропным, иммуномодулирующим, репаративным, ранозаживляющим, отхаркивающим и муколитическим эффектами.