Липопротеины в развитии сердечно-сосудистых заболеваний
Липопротеи́ны в разви́тии серде́чно-сосу́дистых заболева́ний, роль липопротеинов и их различных фракций в развитии сердечно-сосудистых заболеваний.
Структура и функции липопротеинов
Липиды выполняют самые разнообразные функции. Они входят в состав клеточных мембран, служат предшественниками стероидных гормонов, жёлчных кислот, простагландинов и фосфоинозитидов. В крови содержатся отдельные компоненты липидов (насыщенные, моно- и полиненасыщенные жирные кислоты), триглицериды (ТГ), холестерин (ХС), эфиры холестерина и фосфолипиды. Все эти вещества не растворимы в воде, поэтому в организме работает сложная система транспорта липидов. Свободные (неэстерифицированные) жирные кислоты переносятся кровью в виде комплексов с альбумином. Триглицериды, холестерин, эфиры холестерина и фосфолипиды транспортируются в форме водорастворимых липопротеинов.
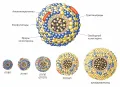
Липопротеины (или липопротеиды) – сферические частицы, состоящие из гидрофобной сердцевины и гидрофильной оболочки. Сердцевина содержит неполярные липиды – триглицериды и эфиры холестерина. Оболочка построена из полярных липидов – холестерина и фосфолипидов, причём заряженные концы этих молекул обращены наружу. Кроме того, в состав оболочки входят белки, нековалентно связанные с фосфолипидами и холестерином, – апопротеины, поддерживающие структуру липопротеиновых частиц и обеспечивающие их взаимодействие с рецепторами липопротеинов.
Циркулируя в крови, липопротеиновые частицы обмениваются между собой поверхностными липидами и апопротеинами. Апопротеины служат «визитной карточкой» липопротеинов, поскольку рецепторы липопротеинов на разных клетках распознают только определённые апопротеины.
Липопротеины подразделяют на несколько классов в зависимости от их плотности (которую оценивают путём ультрацентрифугирования) и подвижности при электрофорезе. Плотность липопротеиновой частицы определяют отношением апопротеины/липиды – чем больше это отношение, тем выше плотность. Подвижность при электрофорезе зависит от содержания апопротеинов и полярных липидов. В крови, взятой натощак, присутствуют только липопротеины очень низкой плотности (ЛПОНП), липопротеины низкой плотности (ЛПНП) и липопротеины высокой плотности (ЛПВП), тогда как другие липопротеины [хиломикроны, остаточные компоненты хиломикронов, а также липопротеины промежуточной плотности (ЛППП)] выявляют только после еды или при нарушениях липидного обмена.
Частицы ЛПНП представляют собой псевдомицеллярные, квазисферические и макромолекулярные комплексы. Липиды составляют около 80 % по массе в этих комплексах, в то же время в протеоме доминирует аполипопротеин aпoB100 (одна молекула на одну частицу ЛПНП). AпoB100 поддерживает структурную целостность частиц в спектре ЛПОНП-ЛПНП и остаётся с частицей липопротеина на протяжении всего его жизненного цикла.
При концентрации циркулирующих частиц в 1 ммоль/л ЛПНП определяют как основной транспортёр ХС, главным образом его эстерифицированной формы. У людей с нормальным уровнем липидов обычно выделяют четыре основных подкласса ЛПНП:
ЛПНП-I (большие лёгкие ЛПНП с плотностью 1,019–1,023 г/мл);
ЛПНП-II (среднего размера с плотностью 1,023–1,034 г/мл);
ЛПНП-III (малого размера с плотностью 1,034–1,044 г/мл);
ЛПНП-IV (очень малого размера с плотностью 1,044–1,063 г/мл), которые присутствуют обычно у лиц с повышенными уровнями триглицеридов.
В то время как в более ранних исследованиях подчёркивали атерогенность малых ЛПНП, ныне считают, что все ЛПНП, независимо от их размера, являются атерогенными. Таким образом, разграничение больших и малых субфракций ЛПНП имеет лишь относительное значение в оценке сердечно-сосудистого риска. Измерение апоВ100 или прямое измерение ЛПНП позволяет определить содержание частиц ЛПНП в плазме крови.
Определение соотношения плазменного уровня общего холестерина (ОХС) к уровню холестерина липопротеинов высокой плотности (ХС ЛПВП) (соотношение ОХС / ХС ЛПВП) предложено в качестве суррогатного маркера атерогенной дислипидемии вместо ЛПНП. Отношение ОХС / ХС ЛПВП может рассматриваться как альтернатива ХС ЛПНП для оценки риска, но не для диагностики или принятия терапевтического решения, потому что в случае высокого содержания ЛПВП пациент может быть ошибочно отнесён к категории низкого риска, даже если у него повышен уровень ХС ЛПНП.
Большинство людей рождаются с уровнем ХС ЛПНП от 40 до 60 мг/дл (1–1,55 ммоль/л). Этот уровень возрастает до 70 мг/дл (1,8 ммоль/л) в течение первых 2 лет жизни, а затем, постепенно повышаясь, достигает 110–120 мг/дл (2,8–3,0 ммоль/л). Уровни ХС ЛПНП достигают плато в среднем возрасте, а затем, в более старшем возрасте, несколько снижаются.
Как правило, уровень ОХС 200 мг/дл соответствует уровню ХС ЛПНП 120 мг/дл (3,0 ммоль/л) и уровню холестерина липопротеинов не высокой плотности (ХС неЛПВП) при оценке концентрации всех циркулирующих и содержащих апоВ липопротеинов 150 мг/дл (3,8 ммоль/л).
Результаты исследований о роли различных классов липопротеинов в развитии сердечно-сосудистых заболеваний
Внутрисосудистые ультразвуковые исследования показали, что прогрессирование атеросклеротических бляшек замедляется при уровне ХС ЛПНП менее 70 мг/дл (1,8 ммоль/л). Следовательно, уровень ХС ЛПНП 70 мг/дл (1,8 ммоль/л) может быть оптимальным уровнем, необходимым для предотвращения прогрессирования атеросклеротической бляшки.
Измерение уровня липидов при рождении и в возрасте 2 лет показано в случае отягощённого семейного анамнеза по ранней ишемической болезни сердца (ИБС) или семейной гиперхолестеринемии (СГХС).
Хотя ХС ЛПНП считают основным фактором в развитии атеросклеротических сердечно-сосудистых заболеваний (АССЗ), имеются убедительные доказательства участия других апoB-содержащих липопротеинов, включая ЛПОНП и липопротеин (а) [Лп(а)], в этом процессе.
Лп(a) вносит вклад не только в атерогенез, но и в атеротромбоз. Приблизительно 20 % населения имеют повышенный уровень Лп(a) в крови, который не зависит от возраста, пола или уровня липидов. Исследования показывают, что до 90 % вариаций уровней Лп(a) в плазме могут быть обусловлены генетическими факторами, что делает Лп(a) наиболее распространённым наследственным фактором риска АССЗ.
В эпидемиологических исследованиях отчётливо показано, что уровень Лп(a) более 50 мг/дл ассоциирован с высоким риском АССЗ. Лп(а) был описан К. Бергом (1932–2009) в 1963 г. как новый антиген плазмы крови, вариант ЛПНП. Лп(а) имеет несколько физических и химических свойств, характерных для ЛПНП, за счёт наличия в его составе холестерина и его эфиров (до 30–45 % от общей массы) и одной молекулы апоВ100, ключевого компонента атерогенных липопротеинов.
Липопротеин (а)
Высокочувствительными методами показано, что Лп(а) можно обнаружить в крови практически всех людей. В редких случаях врождённой абеталипопротеинемии одновременно с апоВ отсутствовал и апоА. Содержание Лп(а) в плазме крови человека варьирует в широких пределах: от едва различимой концентрации до 100 и более мг/дл. Медиана содержания Лп(а) в крови здоровых лиц составляет 12 мг/дл. По другим данным, у ⅔ людей в популяции уровень Лп(а) соcтавляет менее 20 мг/дл, а средний уровень Лп(а) в популяции – 14,0 мг/дл с медианой 8,0 мг/дл. Содержание Лп(а) сразу после рождения очень низкое и нарастает медленно в первые месяцы жизни по сравнению с апоВ. Уровень Лп(а) у детей значительно более низкий, чем у взрослых, и каждый год от рождения до 18 лет содержание Лп(а) в крови увеличивается на 0,9 мг/дл. В дальнейшем уровень Лп(а) сохраняется относительно постоянным и является генетически предопределённым для каждого индивидуума.
Целевого уровня Лп(а) нет, но уровень Лп(a) более 180 мг/дл указывает на очень высокий сердечно-сосудистый риск, Лп(a) более 50 мг/дл – на высокий риск. Рекомендуется измерение ЛП(а) по крайней мере один раз в жизни у каждого взрослого человека, особенно у пациентов с преждевременными атеросклеротическими сердечно-сосудистыми заболеваниями (мужчины до 55 лет, женщины до 60 лет), с семейным анамнезом преждевременного АССЗ и/или с повышенным уровнем Лп(a), семейной гиперхолестеринемией, рецидивирующими АССЗ, несмотря на оптимальное снижение липидов при гиполипидемической терапии.
Аполипопротеин В100
Аполипопротеин В100 (апоВ100) – это белковая часть липопротеинов низкой плотности. Более чем на 90 % ЛПНП состоит из апоB100. АпоВ100 смешан с холестерином в пределах комплекса липопротеинов низкой плотности и, в свою очередь, увеличивает транспортную способность липопротеина низкой плотности с последующим отложением его на артериальной стенке.
Предполагают, что, изучая апоВ100 у пациента, можно получить точный маркер генетической предрасположенности к развитию ИБС. Ген апоВ отмечен на небольшом участке второй хромосомы с приблизительной длиной в 43 килобазы и 29 эксонов. AпoB100 синтезируется в печени и связывается с ЛПОНП. Обмена апоВ100 между липопротеинами не происходит, как это бывает с другими элементами липопротеинов, и он остаётся в ЛПНП и ЛППП после потери ими аполипопротеинов A, E и C. Оценка риска по апоВ100 применима у пациентов с гипертриглицеридемией лёгкой и средней степени тяжести, 2–10 ммоль/л (175–880 мг/дл), диабетом, ожирением или метаболическим синдромом.
Взаимосвязь дислипидемий с риском развития сердечно-сосудистых осложнений
Крупнейшее проспективное исследование MRFIT (Multiple Risk Factor Intervention Trial), проведённое среди 361 662 обследованных мужчин 35–57 лет, позволило определить основные факторы риска ИБС, включая липиды сыворотки крови. Впервые был определён пороговый уровень ОХС (5,2 ммоль/л), начиная с которого регистрировали значительный прирост смертности от ИБС. Абсолютный риск ИБС при самых высоких среднепопуляционных значениях ОХС был в 20 раз выше, чем при наиболее низких уровнях, равных 4,7 ммоль/л.
Метаанализ проспективных эпидемиологических исследований (Фремингемское; MRFIT; Coronary Primary Prevention Trial) выявил зависимость между повышением уровня ХС ЛПВП на 1 мг/дл и снижением на 2–3 % риска ИБС, независимо от других факторов риска, включая ХС ЛПНП.
В метаанализе 17 проспективных популяционных исследований показано, что повышение уровня триглицеридов сыворотки крови на 1 ммоль/л было связано с увеличением новых случаев ИБС на 32 % у мужчин и на 76 % у женщин. По данным крупнейшего эпидемиологического Фремингемского исследования, уровень триглицеридов более 1,7 ммоль/л был связан с более высоким риском развития сердечно-сосудистых осложнений.
При достижении целевого уровня ХС ЛПНП менее 1,8 ммоль/л риск сердечно-сосудистых осложнений у пациентов с ХС ЛПВП менее 1,0 ммоль/л был на 64 % выше, чем у пациентов с ХС ЛПВП 1,4 ммоль/л и выше. Повышенные уровни триглицеридов и низкий уровень ХС ЛПВП синергично увеличивают риск сердечно-сосудистых событий у пациентов с уже достигнутыми целевыми уровнями ХС ЛПНП (менее 2,1 ммоль/л).
Показано, что у пациентов с уровнем триглицеридов более 2,3 ммоль/л и одновременно уровнем ХС ЛПВП менее 0,8 ммоль/л риск сердечно-сосудистых осложнений возрастал в 10 раз по сравнению с пациентами с их нормальными показателями (см. таблицу).
Оптимальные значения показателей липидного профиля в зависимости от категории риска пациента и целевые уровни общего холестерина и его фракций
Параметр | Низкий риск | Умеренный риск | Высокий | Очень высокий риск | |
ОХС | Рекомендовано измерение для расчёта риска по SCORE | ||||
ХС ЛПНП, ммоль/л | < 3,0 | < 2,6 | < 1,8 и снижение ≥ 50 % | < 1,4 и снижение ≥ 50 % | |
ХС ЛПВП, ммоль/л | мужчины > 1,0; женщины > 1,2 | ||||
ХС неЛПВП, ммоль/л |
| < 3,4 | < 2,6 | < 2,2 | |
ТГ, ммоль/л | < 1,7 | ||||
Лп(а), мг/дл | < 50 | < 30 | |||