Галогенфосфины
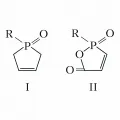
Галогенфосфи́ны, фосфорорганические соединения общей формулы RnPHal3–n (R – углеводородный радикал, n=1, 2). Большинство галогенфосфинов – жидкости с неприятным запахом; растворимы в органических растворителях. Галогенфосфины реагируют с водой и другими соединениями, имеющими в молекуле подвижный атом водорода; легко окисляются на воздухе; CH3PF2 и (CH3)PCl воспламеняются. Благодаря электронодонорной способности галогенфосфины присоединяют серу, галогены, хлорамины (дифторфосфины – также HF, HCl, HOR, H2NR) с образованием различных производных фосфора(V); с переходными металлами образуют комплексные соединения, например Ni(RPF2)4. В присутствии оснований галогенфосфины взаимодействуют с нуклеофильными реагентами с образованием замещённых производных типа RnPX3–n или RP(Hal)X (X–OR, NHR, NR2, SR). С альдегидами и кетонами галогенфосфины образуют α -галогеналкильные производные, например RP(O)ClCHClR, с иминами (в присутствии воды) – α-аминоалкильные производные, с диенами и ненасыщенными карбоновыми кислотами – циклические фосфиноксиды (формула I) и фосфинаты (II). При восстановлении галогенфосфинов в зависимости от условий образуются фосфины, циклополифосфины или дифосфины.
В промышленности алкилдихлорфосфины (в основном CH3PCl2) получают парофазным фосфорилированием углеводородов тригалогенидами фосфора и температуре 300–700 °С (катализаторы – кислород, галогенпроизводные углеводородов, алюмосиликаты) или алкилированием тригалогенидов фосфора металлоорганическими соединениями; ароматические галогенфосфины получают фосфорилированием аренов тригалогенидами фосфора в присутствии AlCl3 или арилированием PHal3 солями арилдиазония.
Галогенфосфины используются в производстве антипиренов, инсектицидов, лекарственных препаратов, экстрагентов, катализаторов, модификаторов полимеров и др.