Металлоорганические соединения
Металлооргани́ческие соедине́ния, химические соединения, содержащие одну или несколько связей металл – углерод; наиболее многочисленна группа элементоорганических соединений. Металлоорганические соединения известны для большинства элементов-металлов. Присоединённые к металлу углеродсодержащие группы называют лигандами. Гомолигандные комплексы, в которых атом металла связан с одинаковыми лигандами, составляют лишь малую часть известных металлоорганических соединений. В подавляющем большинстве металлоорганических соединений с атомом металла связаны лиганды разной природы; это т. н. смешанно-лигандные производные. Металлоорганические соединения могут содержать несколько атомов металла, связанных между собой непосредственно или через мостиковые лиганды, например, железоорганические соединения. Иногда к металлоорганическим соединениям относят органические производные металлов, в которых атом углерода отделён от металла гетероатомом (например, гетерокупраты, медьорганические соединения).
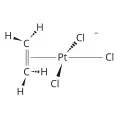
Первым из полученных металлоорганических соединений был комплекс платины с органическими лигандами – соль Цейзе K[PtCl3(C2H4)], синтезированная датским химиком В. Цейзе в 1827 г. В дальнейшем в истории металлоорганических соединений известно несколько качественно новых этапов, важнейшими из которых стали появление универсальных органических реагентов – реактивов Гриньяра в начале 20 в. и открытие ферроцена во 2-й половине 20 в. Практически неограниченные возможности в конструировании новых металлоорганических соединений обусловлены огромным разнообразием известных органических соединений. В природе металлоорганические соединения встречаются очень редко; пример природных металлоорганических соединений – коферментные формы витамина B12.
Классификация металлоорганических соединений включает в себя, помимо собственных, также классификационные признаки органических и координационных соединений. Основными классами следует считать металлоорганические соединения с σ-связью металл – углерод, карбонильные металлоорганические соединения, а также соединения с π-связью между металлом и лигандами – ненасыщенными органическими молекулами. Все остальные металлоорганические соединения обычно рассматриваются как производные представителей одного из этих трёх классов или родственные им.
Органические комплексы, содержащие σ-связи металл – углерод, наиболее характерны для непереходных металлов. В этих металлоорганических соединениях общее число присоединённых к металлу групп обычно хорошо соответствует типичным степеням окисления металла; например, для Sn2+ и Sn4+ это R2Sn и R4Sn, для Tl+ и Tl3+ – RTl и R3Tl; R – одинаковые или разные органические (по крайней мере одна) и неорганические группы. Связи металл – углерод в σ-органических соединениях обычно рассматриваются как двухэлектронные ковалентные. В металлоорганических соединениях других типов, прежде всего в металлоорганических соединениях переходных металлов, характер связи намного сложнее. В них, как правило, реализуются кратные связи металл – лиганд и многоцентровые связи. Так, например, в комплексе бензолхромтрикарбонил связь металл – арен рассматривается как тройная и семицентровая, а связь металл – карбонил как тройная двухцентровая. Исследование типов связей в металлоорганических соединениях сыграло большую роль в развитии представлений о природе химической связи.
Полярность связей металл – лиганд для различных металлоорганических соединений изменяется в широких пределах – от сильно полярной ионной (циклопентадиенид натрия CpNa) до слабо полярной ковалентной (R2Hg, R4Sn, Cp2Fe), и соответственно различаются свойства таких соединений. Большинство металлоорганических соединений высоко реакционноспособные соединения, неустойчивы на воздухе, многие нестабильны при комнатной температуре, некоторые фоточувствительны. Для всех металлоорганических соединений, в т. ч. и для наиболее устойчивых, можно говорить только о кинетической стабильности. Типичными превращениями металлоорганических соединений являются: реакции, затрагивающие только атом металла; реакции, затрагивающие только лиганды; реакции, затрагивающие связь металл – лиганд (в частности, реакции, приводящие к разрушению металлоорганического соединения); комбинированные превращения.
Разнообразие методов синтеза металлоорганических соединений очень велико, однако можно выделить две большие группы этих методов: прямое металлирование, когда связь металл – углерод создаётся впервые, и переметаллирование – когда протекают обменные процессы и для синтеза одних металлоорганических соединений используются другие металлоорганические соединения, полученные заранее.
Многие металлоорганические соединения токсичны (например, ртутьорганические соединения, свинецорганические соединения).
В основном металлоорганические соединения используют как стехиометрические реагенты в тонком органическом синтезе, а также как катализаторы важных промышленных процессов. Чаще всего металлоорганические соединения применяются в процессах, в ходе которых создаются новые связи углерод – углерод и углерод – элемент. Кроме того, некоторые металлоорганические соединения используются в качестве лекарственных препаратов, антиоксидантов, регуляторов процессов горения; оловоорганические соединения – в качестве бактерицидов, фунгицидов и др. На основе металлоорганических соединений создаются новые материалы (в т. ч. анизотропные), использующиеся в высоких технологиях (например, галлийорганические соединения и металлоцены применяют для получения полупроводниковых материалов).