Хелетропные реакции
Хелетро́пные реа́кции (хелотропные реакции; от греч. χηλή – клешня и τρόπος – поворот, направление), частный случай циклоприсоединения (циклораспада), в котором связи образуются (разрываются) синхронно у одного и того же атома. Термин «хелетропные реакции» предложен Р. Б. Вудвордом и Р. Хофманом в 1969 г.
Обычно в хелетропных реакциях образуются две σ-связи между терминальными (концевыми) атомами сопряжённого полиенового субстрата или вицинальными атомами алкенового или алкинового субстратов и атомом реагента, имеющим неподелённую пару электронов в плоскости молекулы и вакантную орбиталь, ортогональную этой плоскости. К таким реагентам относятся SO2, CO, карбены, нитрены, фосфены и т. п. Формально процесс соответствует уменьшению числа π-связей в субстрате и увеличению координационного числа атома реагента. При этом число π-электронов в молекуле уменьшается на 2. Обратную реакцию называют хелетропным элиминированием, хелетропным циклораспадом или экструзией.
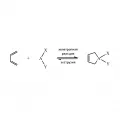 Рис. 1. Хелетропное присоединение молекулы AXY к молекуле диена (прямая реакция) и реакция экструзии (обратная реакция).Различают линейные и нелинейные хелетропные реакции. В линейной реакции орбиталь неподелённой электронной пары атома A участвует по супраповерхностному типу (т. н. σ-сближение реагентов), в нелинейной – по антараповерхностному типу (т. н. π-сближение реагентов) (см. Правила Вудворда – Хофмана).
Рис. 1. Хелетропное присоединение молекулы AXY к молекуле диена (прямая реакция) и реакция экструзии (обратная реакция).Различают линейные и нелинейные хелетропные реакции. В линейной реакции орбиталь неподелённой электронной пары атома A участвует по супраповерхностному типу (т. н. σ-сближение реагентов), в нелинейной – по антараповерхностному типу (т. н. π-сближение реагентов) (см. Правила Вудворда – Хофмана).
Важнейший пример хелетропной реакции – стереоспецифическое присоединение синглетных карбенов к двойной связи с образованием циклопропанов.
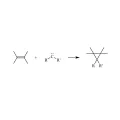 Рис. 2. Присоединение синглетных карбенов к двойной связи.Моделью таких процессов является присоединение синглетного метилена (R=R'=H) к этилену. Высокореакционный шестиэлектронный метилен имеет на атоме углерода вакантную p-орбиталь и двукратно занятую электронами гибридную sp2-орбиталь. При линейном сближении реагентов метилен ориентирован к центру двойной связи С=С вдоль оси симметрии второго порядка. В этом случае перициклическое трёхцентровое переходное состояние формируется четырьмя электронами.
Рис. 2. Присоединение синглетных карбенов к двойной связи.Моделью таких процессов является присоединение синглетного метилена (R=R'=H) к этилену. Высокореакционный шестиэлектронный метилен имеет на атоме углерода вакантную p-орбиталь и двукратно занятую электронами гибридную sp2-орбиталь. При линейном сближении реагентов метилен ориентирован к центру двойной связи С=С вдоль оси симметрии второго порядка. В этом случае перициклическое трёхцентровое переходное состояние формируется четырьмя электронами.
 Рис. 3. Орбитальные взаимодействия в переходных состояниях линейного и нелинейного хелетропного присоединения синглетного метилена к этилену.В соответствии с обобщённым правилом отбора Вудворда – Хофмана в термически разрешённых перициклических реакциях общее число (4q + 2) супра-компонент и (4r) антараповерхностных должно быть нечётным (q, r = 0, 1, 2…). В рассматриваемом линейном хелетропном процессе общее число супра-компонент равно 2, а антара-компоненты требуемого вида отсутствуют, поэтому линейный процесс в термических условиях запрещён по симметрии.
Рис. 3. Орбитальные взаимодействия в переходных состояниях линейного и нелинейного хелетропного присоединения синглетного метилена к этилену.В соответствии с обобщённым правилом отбора Вудворда – Хофмана в термически разрешённых перициклических реакциях общее число (4q + 2) супра-компонент и (4r) антараповерхностных должно быть нечётным (q, r = 0, 1, 2…). В рассматриваемом линейном хелетропном процессе общее число супра-компонент равно 2, а антара-компоненты требуемого вида отсутствуют, поэтому линейный процесс в термических условиях запрещён по симметрии.
В нелинейном процессе метилен приближается к этилену боком, участвуя в реакции не только супра-поверхностно (благодаря гибридной двухэлектронной орбитали), но ещё и антара-поверхностно из-за наличия вакантной р-орбитали (r = 0). Общее число двухэлектронных супра-компонент равно 2, число нольэлектронных антара-компонент равно 1, общее число компонент (2 + 1 = 3) нечётное, и нелинейный термический процесс разрешён по симметрии.
К тем же выводам можно прийти, рассматривая π-электроны, участвующие в формировании перициклического переходного состояния. Линейные хелетропные реакции сопровождаются дисротаторным вращением концевых групп, когда число π-электронов n = 4q, и конротаторным при n = 4q + 2, нелинейные – конротаторным вращением при n = 4q и дисротаторным при n = 4q + 2 (для линейного присоединения метилена к этилену n = 4q + 2 = 2).
Число π-электронов | Термическая реакция | |
4q*; (4q + 2)** | Линейная | Нелинейная |
(4q + 2)*; 4q** | Нелинейная | Линейная |
* Присоединение. | ||
** Экструзия. | ||
Присоединение нитренов к олефинам приводит к азиридинам. Так, синглетный пентафторфенилнитрен с транс-стильбеном даёт соответствующий транс-азиридин; цис-стильбен дает цис-азиридин.
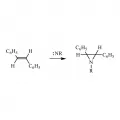 Рис. 4. Хелетропное присоединение синглетного пентафторфенилнитрена (R = C₆F₅N) к транс-стильбену с образованием азиридина.Аналогично протекает реакция с атомарным кислородом с образованием оксиранов.
Рис. 4. Хелетропное присоединение синглетного пентафторфенилнитрена (R = C₆F₅N) к транс-стильбену с образованием азиридина.Аналогично протекает реакция с атомарным кислородом с образованием оксиранов.
В случае силиленов и гермиленов гетероциклические аддукты образуются лишь на промежуточных стадиях реакций.
 Рис. 5. Хелетропное присоединение синглетного силилена к этилену.С диеновыми системами синглетные карбены образуют винилциклопропаны, а триплетные – циклопентены.
Рис. 5. Хелетропное присоединение синглетного силилена к этилену.С диеновыми системами синглетные карбены образуют винилциклопропаны, а триплетные – циклопентены.
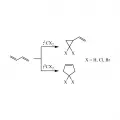 Рис. 6. Хелетропное присоединение синглетного (¹CX₂) и триплетного карбенов (³CX₂) к диену.Хелетропные реакции силиленов и гермиленов с диенами приводят к продуктам 1,4-циклоприсоединения, а реакции с цис-1,3,5-гексатриеном – к продуктам 1,6-циклоприсоединения. Хелетропные реакции карбенов с ацетиленами – один из основных методов получения производных циклопропена.
Рис. 6. Хелетропное присоединение синглетного (¹CX₂) и триплетного карбенов (³CX₂) к диену.Хелетропные реакции силиленов и гермиленов с диенами приводят к продуктам 1,4-циклоприсоединения, а реакции с цис-1,3,5-гексатриеном – к продуктам 1,6-циклоприсоединения. Хелетропные реакции карбенов с ацетиленами – один из основных методов получения производных циклопропена.
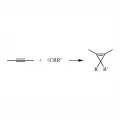 Рис. 7. Хелетропное присоединение карбена к тройной связи.Хелетропные реакции нитренов с ацетиленами приводят к азиринам. Силилены и гермилены с алкинами могут образовывать в качестве промежуточных продуктов сила- и гермациклопропены, которые превращаются в циклические шестичленные аддукты.
Рис. 7. Хелетропное присоединение карбена к тройной связи.Хелетропные реакции нитренов с ацетиленами приводят к азиринам. Силилены и гермилены с алкинами могут образовывать в качестве промежуточных продуктов сила- и гермациклопропены, которые превращаются в циклические шестичленные аддукты.
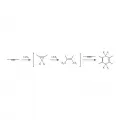 Рис. 8. Хелетропное присоединение силилена (A = Si) и гермилена (A = Ge) к тройной связи. В квадратных скобках показаны возможные интермедиаты.Наиболее широко распространены хелетропные реакции распада циклических структур с выбросом (экструзией) небольших молекул типа SO2, N2, CO и др. Так, элиминирование N2 из циклических диазенов протекает стереоспецифично.
Рис. 8. Хелетропное присоединение силилена (A = Si) и гермилена (A = Ge) к тройной связи. В квадратных скобках показаны возможные интермедиаты.Наиболее широко распространены хелетропные реакции распада циклических структур с выбросом (экструзией) небольших молекул типа SO2, N2, CO и др. Так, элиминирование N2 из циклических диазенов протекает стереоспецифично.
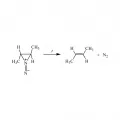 Рис. 8. Экструзия N₂ из циклического диазена.В термически разрешённой линейной хелетропной реакции дисротаторного раскрытия цикла транс-сульфонов образуются цис-транс-диены, а из цис-сульфонов – транс-транс-диены.
Рис. 8. Экструзия N₂ из циклического диазена.В термически разрешённой линейной хелетропной реакции дисротаторного раскрытия цикла транс-сульфонов образуются цис-транс-диены, а из цис-сульфонов – транс-транс-диены.
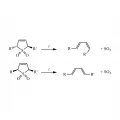 Рис. 9. Экструзия SO₂ из сульфонов.Аналогично протекает реакция для транс-диазенов.
Рис. 9. Экструзия SO₂ из сульфонов.Аналогично протекает реакция для транс-диазенов.
