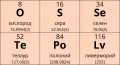
Халькогены
Халькоге́ны, химические элементы VI группы короткой формы (16-й группы длинной формы) периодической системы: кислород, сера, селен, теллур, полоний и искусственно полученный элемент ливерморий. Термин «халькогены» происходит от греч. χαλϰός – медь, руда и γενής – рождающий: по нахождению элементов в природе в составе медных руд (например, сульфидных). Бинарные соединения халькогенов с металлами – т. н. халькогениды.
Внешняя электронная оболочка атомов халькогенов имеет конфигурацию s2p4. С увеличением атомного номера в ряду элементов O – S – Se – Te – Po возрастают ковалентные и ионные радиусы, уменьшаются энергия ионизации атома и энергия диссоциации молекулы Х2, падает электроотрицательность, усиливаются металлические свойства, неметаллические свойства закономерно ослабляются. Так, Po проявляет некоторые свойства, характерные для металлов (образует одноатомные катионы, реагирует с кислотами с выделением водорода и т. п.). Общее свойство всех халькогенов – склонность к катенации (образование связей Э–Э в соединениях), которая реализуется как в простых веществах (например, озон O3, сера S8), так и в соединениях (пентасульфид натрия Na2S5, тиосульфат натрия Na2S2O3 и т. п.). Характерные степени окисления халькогенов: –2, –1, +1, +2, а также +4 и +6 для всех, кроме кислорода.