Электроциклические реакции
Электроцикли́ческие реа́кции, внутримолекулярные перициклические реакции, в которых образуется новая σ-связь между концами линейных молекул или их отдельных линейных участков, представляющих собой сопряжённые системы. При этом число π-связей уменьшается на единицу.
Термин «электроциклические реакции» введён Р. Вудвордом и Р. Хофманом в 1969 г.
Типичные примеры – электроциклизация гексатриена-1,3,5 в циклогексадиен и реакция Назарова:
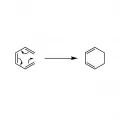 Электроциклизация гексатриена-1,3,5 в циклогексадиен.
Электроциклизация гексатриена-1,3,5 в циклогексадиен.
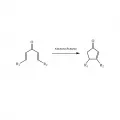 Реакция Назарова.К электроциклическим реакциям относят также обратный процесс раскрытия цикла с разрывом σ-связи и образованием сопряжённой системы, например раскрытие циклобутена в бутадиен:
Реакция Назарова.К электроциклическим реакциям относят также обратный процесс раскрытия цикла с разрывом σ-связи и образованием сопряжённой системы, например раскрытие циклобутена в бутадиен:
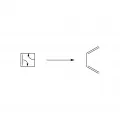 Электроциклическое раскрытие циклобутена в бутадиен.Существует два стереохимически различных пути электроциклических реакций – конротаторный и дисротаторный (см. в статье Правила Вудворда – Хофмана). Электроциклические реакции могут быть как фотохимическими, так и термическими.
Электроциклическое раскрытие циклобутена в бутадиен.Существует два стереохимически различных пути электроциклических реакций – конротаторный и дисротаторный (см. в статье Правила Вудворда – Хофмана). Электроциклические реакции могут быть как фотохимическими, так и термическими.
Простейшая электроциклическая реакция – раскрытие циклопропенильного катиона с образованием аллильного катиона (2π-электронная система), осуществляющееся в условиях сольволиза дисротаторным путём.
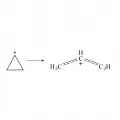 Электроциклическое превращение циклопропильного катиона в аллил-катион.Если трёхчленный цикл входит в бициклическую систему, то его раскрытие зависит от размера второго цикла и положения уходящей группы относительно плоскости трёхчленного цикла. Для эндо-производных сольволиз протекает быстрее, чем для экзо-изомеров (в случае моноциклических циклопропанов этот эффект выражен слабее).
Электроциклическое превращение циклопропильного катиона в аллил-катион.Если трёхчленный цикл входит в бициклическую систему, то его раскрытие зависит от размера второго цикла и положения уходящей группы относительно плоскости трёхчленного цикла. Для эндо-производных сольволиз протекает быстрее, чем для экзо-изомеров (в случае моноциклических циклопропанов этот эффект выражен слабее).
Подробно изучена электроциклическая реакция превращения циклобутена в 1,3-бутадиен (4π-электронная система), проходящая в термических условиях по конротаторному механизму. Реакции высокостереоспецифичны: из цис-3,4-диметилциклобутенов получают только цис, транс-гексадиены, а из транс-изомеров – только транс, транс-гексадиены.
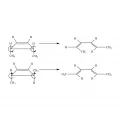 Электроциклическое превращение циклобутена в 1,3-бутадиен.Стереоспецифичность превращений легко объясняется построением корреляционных диаграмм молекулярных орбиталей или электронных состояний. Применение метода граничных орбиталей Фукуи предполагает разбиение исходной циклической системы на два фрагмента и построение на каждом из них высшей заполненной молекулярной орбитали (ВЗМО) и низшей свободной молекулярной орбитали (НСМО) (см. в статье Теория граничных орбиталей). Например, в случае термического раскрытия кольца 3,4-диметилциклобутена следует рассмотреть два разных сочетания граничных орбиталей – для разрываемой σ-связи и этиленового фрагмента.
Электроциклическое превращение циклобутена в 1,3-бутадиен.Стереоспецифичность превращений легко объясняется построением корреляционных диаграмм молекулярных орбиталей или электронных состояний. Применение метода граничных орбиталей Фукуи предполагает разбиение исходной циклической системы на два фрагмента и построение на каждом из них высшей заполненной молекулярной орбитали (ВЗМО) и низшей свободной молекулярной орбитали (НСМО) (см. в статье Теория граничных орбиталей). Например, в случае термического раскрытия кольца 3,4-диметилциклобутена следует рассмотреть два разных сочетания граничных орбиталей – для разрываемой σ-связи и этиленового фрагмента.
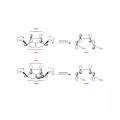 Конротаторное раскрытие 3,4-диметилциклобутена в термических условиях. В одном случае на разрываемой С−С-связи локализована ВЗМО, в другом случае – НСМО.Независимо от выбора граничной орбитали на разрывающейся связи имеет место чёткая корреляция орбитали σ-связи и граничной орбитали продукта (бутадиена-1,3) на конротаторном пути процесса.
Конротаторное раскрытие 3,4-диметилциклобутена в термических условиях. В одном случае на разрываемой С−С-связи локализована ВЗМО, в другом случае – НСМО.Независимо от выбора граничной орбитали на разрывающейся связи имеет место чёткая корреляция орбитали σ-связи и граничной орбитали продукта (бутадиена-1,3) на конротаторном пути процесса.
В случае бициклобугенов, в соответствии с правилами Вудворда – Хофмана, конротаторное раскрытие колец должно приводить к стерически напряжённым цис, транс-циклодиенам, содержащим транс-сочленённую двойную связь. Поэтому для бициклоалкенов при n⩽4 предпочтителен запрещённый механизм раскрытия, приводящий к цис, цис-циклодиенам.
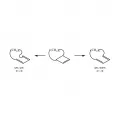 Электроциклическое раскрытие бициклобутенов.Фотохимические взаимопревращения бутадиенов и циклобутенов протекают по дисротаторному механизму.
Электроциклическое раскрытие бициклобутенов.Фотохимические взаимопревращения бутадиенов и циклобутенов протекают по дисротаторному механизму.
В электроциклических реакциях участвуют другие 4π-электронные системы, например трёхчленные циклы, содержащие гетероатом с неподелённой электронной парой; раскрытие кольца для этих систем протекает в термических условиях по конротаторному механизму.
Термически дисротаторная циклизация транс, цис, транс-2,4,6-октатриена (6π-электронная система) приводит почти исключительно к цис-5,6-диметил-1,3-циклогексадиену. Фотохимическая циклизация протекает конротаторно с образованием транс-изомера:
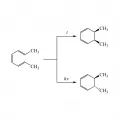 Циклизация 2,4,6-октатриена в термических и фотохимических условиях.Циклические триеновые системы в условиях термических электроциклических реакций находятся в равновесии с бициклическим продуктом, при этом чем более напряжена структура бициклических соединений (т. е. чем меньше n), тем в большей степени равновесие сдвинуто в сторону моноциклической структуры.
Циклизация 2,4,6-октатриена в термических и фотохимических условиях.Циклические триеновые системы в условиях термических электроциклических реакций находятся в равновесии с бициклическим продуктом, при этом чем более напряжена структура бициклических соединений (т. е. чем меньше n), тем в большей степени равновесие сдвинуто в сторону моноциклической структуры.
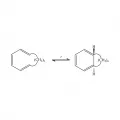 Равновесие циклических и бициклических триенов.Электроциклические реакции с участием 8π-электронных систем протекают при нагревании по конротаторному механизму, например:
Равновесие циклических и бициклических триенов.Электроциклические реакции с участием 8π-электронных систем протекают при нагревании по конротаторному механизму, например:
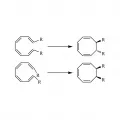 Электроциклические реакции с участием 8π-электронных систем.Электроциклические реакции широко представлены в органическом синтезе и часто встречаются в природе (например, в биосинтезах витамина D₃ и аранотина, в превращениях терпенов и др.).
Электроциклические реакции с участием 8π-электронных систем.Электроциклические реакции широко представлены в органическом синтезе и часто встречаются в природе (например, в биосинтезах витамина D₃ и аранотина, в превращениях терпенов и др.).
